Questões de Química - Representação das transformações químicas para Concurso
Foram encontradas 1.297 questões
1 torr ≅ 133 Pa; 1 bar ≅ 14,5 psi; 1 psi ≅ 7,0 kPa
Considerando-se essas relações, 210,5 torr correspondem, aproximadamente, ao seguinte valor em psi:
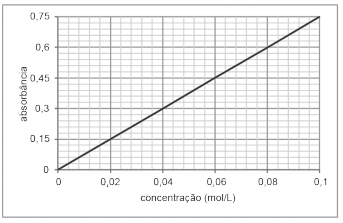
Uma amostra correspondendo a uma solução aquosa contendo Cu+2 passou pelo seguinte procedimento: uma alíquota de 10 mL dessa amostra foi completamente diluída em água até atingir um volume final de solução de 50 mL; uma alíquota dessa solução foi analisada no espectrômetro obtendo-se uma absorbância igual a 0,45.
A concentração de Cu+2 na amostra inicial, em mol L-1 , é
A amostra reagiu com uma solução de íons oxalato em excesso, acarretando a precipitação de MgC2 O4 , conforme apresentado na reação I. Considere que o magnésio foi o único componente da amostra a precipitar.
Em seguida, o precipitado foi filtrado, lavado e calcinado (reação II), gerando uma amostra sólida de 3,05 g.
Reação I: Mg2+ (aq) + C2 O4 2- (aq) → MgC2 O4 (s)
Reação II: MgC2 O4 (s) → MgO (s) + CO (g) + CO2 (g)
A concentração, em g L-1, de magnésio na amostra é
Dado massas molares: Mg = 24 g mol-1 , O = 16 g mol-1 , C = 12 g mol-1
Nesse processo, a massa de eteno, em quilogramas, necessária para produzir 8.720 kg de bromoetano é igual a
Dado massas molares: C = 12 g mol-1 , H = 1 g mol-1, Br = 80 g mol-1
CaCO3 (s) + 2 HCl(aq) → CaCl2 (aq) + H2 O(l) + CO2 (g)
Nessa análise, as impurezas presentes não reagiram e houve o completo consumo do carbonato de cálcio, com formação de 0,66 g de CO2 .
O grau de pureza do carbonato de cálcio na amostra é igual a
Dado
massas molares: Ca = 40 g mol-1,
C = 12 g mol-1, H = 1 g mol-1,
O = 16 g mol-1, Cl = 35,5 g mol-1