Questões de Química - Cinética Química para Concurso
Foram encontradas 403 questões
Catalisadores são substâncias utilizadas para aumentar a energia de ativação de reações químicas.
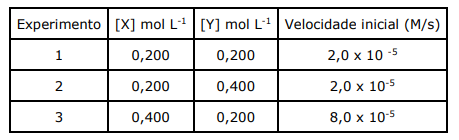
Com base nos dados da tabela, analise as assertivas abaixo:
I. A lei de velocidade para a reação é v= k [X]2 .
II. A concentração de Y não tem nenhum efeito sobre a velocidade da reação.
III. A ordem global da reação é 3.
IV. A constante de velocidade da reação é 2,0 x 10-3 M-1s-1.
Quais estão corretas?
Tabela: Dados obtidos na investigação cinética (método da velocidade inicial) para a reação: 2 A2B(g) → 2 A2(g) + B2(g).
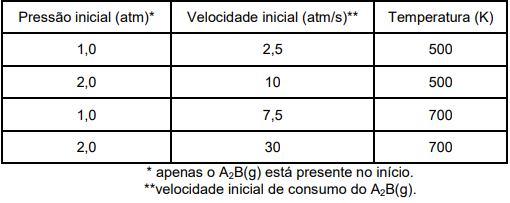
Diante das informações acima, assinale a opção que mostra A VELOCIDADE DA REAÇÃO (em termos de consumo do A2B(g)), em atm/s, quando a pressão de A2B(g) é igual a 1,5 atm à temperatura de 600 K: