Questões de Vestibular de Química - Equilíbrio Químico
Foram encontradas 632 questões
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784291
Química
A combustão incompleta de substâncias, contendo carbono, pode formar o monóxido de carbono, o
qual é extremamente tóxico. O monóxido de carbono, na presença de oxigênio, pode ser convertido
no dióxido de carbono, em catalisadores automotivos, de acordo com a reação abaixo.
2 CO (g) + O2 (g) ⇋ 2 C02 (g)
Em um determinado recipiente, contendo inicialmente monóxido de carbono e oxigênio, estabeleceuse um equilíbrio em que se pode determinar a pressão total da mistura, 6,1 atm, e as pressões parciais de monóxido de carbono e de dióxido de carbono, as quais foram, respectivamente, 0,5 atm e 4,0 atm.
O valor da constante de equilíbrio será igual a
2 CO (g) + O2 (g) ⇋ 2 C02 (g)
Em um determinado recipiente, contendo inicialmente monóxido de carbono e oxigênio, estabeleceuse um equilíbrio em que se pode determinar a pressão total da mistura, 6,1 atm, e as pressões parciais de monóxido de carbono e de dióxido de carbono, as quais foram, respectivamente, 0,5 atm e 4,0 atm.
O valor da constante de equilíbrio será igual a
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784289
Química
Em altas temperaturas, o hidrogênio molecular pode estar em equilíbrio com o hidrogênio atômico
através da seguinte reação
H2(g) ⇋ 2 H (g)
Sobre essa reação, são feitas as seguintes afirmações.
I - A quantidade de hidrogênio atômico aumenta com o aumento da temperatura, porque a reação é endotérmica. II - Em condições de baixa temperatura, não há energia suficiente para romper a ligação. III- A variação de entalpia envolvida na reação é o dobro da entalpia de formação do hidrogênio atômico nas condições da reação.
Quais estão corretas?
H2(g) ⇋ 2 H (g)
Sobre essa reação, são feitas as seguintes afirmações.
I - A quantidade de hidrogênio atômico aumenta com o aumento da temperatura, porque a reação é endotérmica. II - Em condições de baixa temperatura, não há energia suficiente para romper a ligação. III- A variação de entalpia envolvida na reação é o dobro da entalpia de formação do hidrogênio atômico nas condições da reação.
Quais estão corretas?
Ano: 2019
Banca:
UFRGS
Órgão:
UFRGS
Prova:
UFRGS - 2019 - UFRGS - Vestibular - UFRGS - Biologia, Química e Geografia |
Q1784286
Química
Uma suspensão de sulfato de bário pode ser usada como agente de contraste em exames de raios-X. O
sulfato de bário é um sal pouco solúvel, com constante do produto de solubilidade 1,1 x 10-10•
Em relação a uma solução aquosa saturada desse sal, contendo uma certa quantidade de sal sólido, não dissolvido, são feitas as seguintes afirmações.
I - A adição de nitrato de bário diminui a quantidade de sólido não dissolvido. II - A adição de sulfato de sódio aumenta a quantidade de sólido não dissolvido. III - Uma reação reversível, na qual a dissolução do sal é exatamente contrabalançada pela sua precipitação, é estabelecida nessa situação.
Quais estão corretas?
Em relação a uma solução aquosa saturada desse sal, contendo uma certa quantidade de sal sólido, não dissolvido, são feitas as seguintes afirmações.
I - A adição de nitrato de bário diminui a quantidade de sólido não dissolvido. II - A adição de sulfato de sódio aumenta a quantidade de sólido não dissolvido. III - Uma reação reversível, na qual a dissolução do sal é exatamente contrabalançada pela sua precipitação, é estabelecida nessa situação.
Quais estão corretas?
Q1783360
Química
Uma solução de hidróxido de potássio foi preparada pela dissolução de 0,056 g de KOH em água destilada,
obtendo-se 100 mL dessa mistura homogênea.
Dado: MM (KOH) = 56 g.mol-1
De acordo com as informações apresentadas, verifica-se que essa solução apresenta
Dado: MM (KOH) = 56 g.mol-1
De acordo com as informações apresentadas, verifica-se que essa solução apresenta
Q1770256
Química
O ânion fenolato, empregado na produção de corantes, é formado na ionização do fenol em
solução aquosa, conforme representado abaixo:
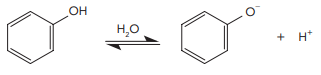
Considere um processamento no qual houve a dissolução completa de 0,01 mol de fenol em água para formar 1 L de solução a 20 °C. Nessa temperatura, a constante de acidez do fenol é igual a 10−10. Atingido o equilíbrio químico da ionização, a concentração de ânion fenolato, em mol/L, na solução, é aproximadamente igual a:

Considere um processamento no qual houve a dissolução completa de 0,01 mol de fenol em água para formar 1 L de solução a 20 °C. Nessa temperatura, a constante de acidez do fenol é igual a 10−10. Atingido o equilíbrio químico da ionização, a concentração de ânion fenolato, em mol/L, na solução, é aproximadamente igual a:
