Questões de Vestibular de Química - Sistemas Gasosos - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro.
Foram encontradas 235 questões
Com relação a princípios da química, julgue o próximo item.
Considere que 1 K = 1 ° C + 273, se o ar no interior de um pneu está a 15 ° C sob a pressão de 5 atm, então a pressão será maior que 5,5 atm quando o ar estiver a 38 ° C.
A respeito das substâncias e de suas transformações químicas, julgue o item a seguir.
Mantendo o volume constante, a pressão de um gás ideal aumentará se houver aumento da temperatura.
O gás hidrogênio foi usado no dirigível rígido Graff Zeppelin. Já o gás hélio é atualmente usado nos dirigíveis semirrígidos e não rígidos.
Sobre esses gases, é CORRETO afirmar que ambos são
(Dados: N = 14 g.mol-1; H = 1 g.mol-1; R = 0,082 atm.L.mol-1.K-1)
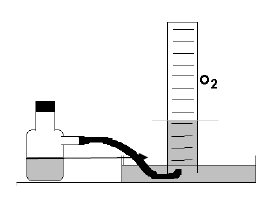
Água oxigenada contém peróxido de hidrogênio (H2O2), que, com o uso de um catalisador, se decompõe, produzindo gás oxigênio e água, conforme a equação abaixo.
H2O2 H2O + ½ O2
Um grupo de estudantes fizeram essa experiência, usando 100 mL de água oxigenada, coletando o gás oxigênio obtido sobre água, conforme ilustrado pela figura, obtendo 1,17 L de gás oxigênio, medidos a uma pressão atmosférica de 0,91atmosferas e a uma temperatura de 20 oC .
Usando a equação PV=nRT, conseguiram determinar o número de mols de O2 obtido e, consequentemente, o número de mols de H2O2 contidos no volume de água oxigenada utilizada. Dessa forma, puderam também determinar a massa deH2O2 contidos nessa água oxigenada. Diante do exposto, pode se concluir que a percentagem m/v (massa volume) deH2O2 na água oxigenada é:
Dados: Constante dos gases ideais R=0,082 atm.L/mol.KK = 273 + t (oC)
