Questões de Vestibular de Química - Sistemas Gasosos - Lei, Teoria Cinética, Equação e Mistura dos Gases. Princípio de Avogadro.
Foram encontradas 235 questões
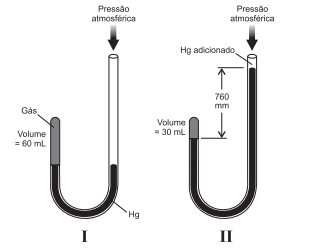
O químico inglês Robert Boyle investigou a relação entre a pressão de uma massa gasosa e seu volume à temperatura constante. Para atingir esse objetivo, realizou uma série de experiências utilizando um manômetro em forma de “jota” com uma extremidade aberta, como mostra a figura I e II. Boyle variou a pressão sobre o gás adicionando mercúrio dentro do tubo e, com os dados experimentais, estabeleceu uma relação empírica entre pressão e volume de uma massa gasosa.
Admitindo-se que o gás utilizado por Boyle é ideal, uma análise
dessas considerações permite afirmar:

CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

 e
e  são as velocidades
características das moléculas de H2 e O2,
respectivamente. A seguir, assinale o que for
correto.
são as velocidades
características das moléculas de H2 e O2,
respectivamente. A seguir, assinale o que for
correto.
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

 e
e  são as velocidades
características das moléculas de H2 e O2,
respectivamente. A seguir, assinale o que for
correto.
são as velocidades
características das moléculas de H2 e O2,
respectivamente. A seguir, assinale o que for
correto.
CLASSIFICAÇÃO PERIÓDICA DOS ELEMENTOS
COM MASSAS ATÔMICAS REFERIDAS AO ISÓTOPO 12 DO CARBONO

 e
e  são as velocidades
características das moléculas de H2 e O2,
respectivamente. A seguir, assinale o que for
correto.
são as velocidades
características das moléculas de H2 e O2,
respectivamente. A seguir, assinale o que for
correto.
Em frascos de água oxigenada, a concentração dessa é expressa em volumes, como água oxigenada a 10 volumes, a 20 volumes etc. Essa concentração corresponde ao número de litros de gás oxigênio medido nas condições normais de temperatura e pressão (CNTP), obtidos pela decomposição completa de todo H2O2 em um litro de solução. Considerando que a reação abaixo transcorra na CNTP e que R = 0,082 atm.L.mol-1K-1, assinale o que for correto.
 1 H2O(l) + 1/2 O2(g)
1 H2O(l) + 1/2 O2(g)