Questões de Vestibular de Química - Equilíbrio Químico
Foram encontradas 633 questões
O uso do ácido acetil salicílico como princípio ativo de medicamentos analgésicos é bastante comum. Ao ser ingerida, essa substância se dissocia no estômago, em uma reação que apresenta equilíbrio químico. A equação abaixo representa a reação de dissociação do ácido acetil salicílico, cuja fórmula é representada de forma simplificada por HAs.
HAs(aq) ⇌ H+ (aq) + As- (aq).
O organismo humano absorve apenas a forma dissociada dessa substância, sendo o íon As- o responsável pelo efeito analgésico.
O procedimento que acelera a absorção do medicamento pelo organismo é
Um refrigerante é uma solução homogênea e líquida enquanto está contido em um frasco fechado. Quando se abre esse frasco, bolhas de gás surgem imediatamente, emergindo do líquido para a superfície. Esse gás é o dióxido de carbono que interage com a água segundo o equilíbrio:
CO2 (g) + H2O (l) ⇆ H2CO3 (aq).A opção que apresenta, corretamente, o deslocamento do equilíbrio da reação representada
é:
Observe a escala abaixo:

O suco extraído do repolho roxo pode ser utilizado como indicador do caráter ácido (pH entre 0 e 7) ou básico (pH entre 7 e 14) de diferentes soluções. Misturando-se um pouco de suco de repolho e da solução, a mistura passa a apresentar diferentes cores, segundo sua natureza ácida ou básica, de acordo com a escala acima, que relaciona a cor final do sistema substância + indicador com o pH aproximado que ela possui. Ao testar algumas soluções com o suco de repolho roxo, foram obtidos os seguintes resultados:
- Amoníaco: verde
- Leite de magnésia: azul
- Vinagre: vermelho
- Leite de vaca: rosa
Com base nessas informações, as substâncias amoníaco, leite de magnésia, vinagre e
leite de vaca têm caráter respectivamente:
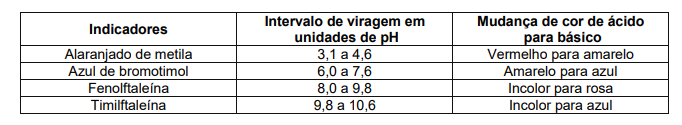
Para diferenciar-se uma solução de pH=5,0 de uma solução de pH=8,0, ambas incolores, deve-se usar o indicador
Com base na expressão
NH4+(aq) ⇄ H+(aq) + NH3(aq)
que representa a solução aquosa do (NH4)Cℓ , é correto afirmar que: