Questões de Química - Fórmulas, Balanceamento e Leis ponderais das reações químicas para Concurso
Foram encontradas 541 questões
Ano: 2023
Banca:
FUNDATEC
Órgão:
GHC-RS
Prova:
FUNDATEC - 2023 - GHC-RS - Engenheiro (Engenharia Química) |
Q2176448
Química
A queima completa do acetileno gasoso (C2H2) gera, como produtos formados, gás
carbônico gasoso (CO2) e água (H2O). Considerando essa reação química, para fornecer 17,5 mol de
água, qual deverá ser a quantidade de matéria (em mol) necessária de gás oxigênio?
Ano: 2023
Banca:
SELECON
Órgão:
IF-RJ
Prova:
SELECON - 2023 - IF-RJ - Técnico de Laboratório/Química |
Q2175675
Química
Os fosfatos encontrados na natureza não são suficientes
para serem utilizados como fertilizantes. Para a produção
comercial de fertilizantes fosfatados, o mineral fluorapatita pode
ser empregado para tratamento com ácido fosfórico (I) resultando
em di-hidrogenofosfato de cálcio monohidratado e ácido
fluorídrico, conforme demonstrado pela reação, não balanceada,
a seguir.
Ca5(PO4)3 F + H3PO4 + H2O HF + Ca(H2PO4)2 . H2O (I)
Em um processo industrial, partiu-se de 1 tonelada de fluorapatita fazendo-a reagir com uma quantidade suficiente de ácido fosfórico obtendo-se, ao final, 2 toneladas do produto di-hidrogenofosfato de cálcio monohidratado. Pode-se, por esses dados, prever que a pureza do mineral utilizado, em percentual, era aproximadamente igual a:
(Dados, em g/mol: Ca= 40, P=31, O=16, H=1, F=19)
Ca5(PO4)3 F + H3PO4 + H2O HF + Ca(H2PO4)2 . H2O (I)
Em um processo industrial, partiu-se de 1 tonelada de fluorapatita fazendo-a reagir com uma quantidade suficiente de ácido fosfórico obtendo-se, ao final, 2 toneladas do produto di-hidrogenofosfato de cálcio monohidratado. Pode-se, por esses dados, prever que a pureza do mineral utilizado, em percentual, era aproximadamente igual a:
(Dados, em g/mol: Ca= 40, P=31, O=16, H=1, F=19)
Ano: 2023
Banca:
SELECON
Órgão:
IF-RJ
Prova:
SELECON - 2023 - IF-RJ - Técnico de Laboratório/Química |
Q2175663
Química
O octano (C8H18) é um hidrocarboneto constituinte da 8 18
gasolina. A reação não balanceada da combustão completa do
octano segue abaixo:
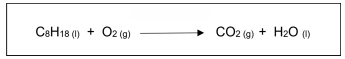
Para queimar completamente 2,00 mols de octano, serão necessários:

Para queimar completamente 2,00 mols de octano, serão necessários:
Ano: 2023
Banca:
UERJ
Órgão:
UERJ
Prova:
UERJ - 2023 - UERJ - Técnico Universitário Superior - Químico |
Q2167527
Química
Para determinar o teor de ácido oxálico em uma planta, foi realizada uma extração seguida de uma
titulação com solução padronizada de permanganato de potássio. Nessa titulação, ocorre a seguinte
reação não balanceada do permanganato com ácido oxálico em meio ácido:
(MnO4) - (aq) + H2C2O4(aq) + H+ (aq) → Mn2+(aq) + H2O(l) + CO2(g)
A soma dos menores coeficientes inteiros que balanceiam a equação é:
(MnO4) - (aq) + H2C2O4(aq) + H+ (aq) → Mn2+(aq) + H2O(l) + CO2(g)
A soma dos menores coeficientes inteiros que balanceiam a equação é:
Ano: 2023
Banca:
UERJ
Órgão:
UERJ
Prova:
UERJ - 2023 - UERJ - Técnico Universitário Superior - Químico |
Q2167517
Química
Na gravimetria por precipitação, o analito é convertido em um precipitado pouco solúvel e, então,
esse precipitado é filtrado, lavado, convertido em um produto de composição conhecida por meio de um
tratamento térmico adequado e pesado. Um exemplo é o método oficial da Associação Oficial de Química
Analítica, em que, a partir do ácido oxálico, H2C2O4, tem-se a precipitação do oxalato de cálcio (CaC2O4).
A espécie química sólida obtida após o processo de calcinação do oxalato de cálcio tem como fórmula: