Questões de Vestibular de Química - Velocidade de Reação, Energia de Ativação, Concentração, Pressão, Temperatura e Catalisador
Foram encontradas 268 questões
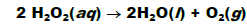
Na presença do íon brometo (Br- ), a decomposição ocorre rapidamente segundo as reações:
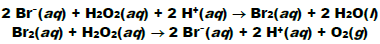
As reações vistas podem ser demonstradas graficamente a partir de um diagrama de energia potencial:
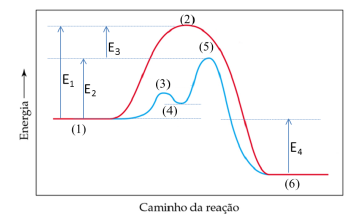
Em relação à decomposição do H2O2:
I. A reação sem catalisador acontece em apenas uma etapa e a reação com catalisador acontece em duas etapas, porém o produto formado é exatamente o mesmo.
II. E1 é a energia de ativação referente à decomposição do H2O2 na ausência de catalisador e E3 é a energia de ativação referente à decomposição do H2O2 na presença de catalisador. III. E2 é a energia de ativação da etapa determinante da velocidade da reação catalisada pelo íon Br- .
IV. E4 é a variação de entalpia da reação, que é endotérmica.
V. No gráfico, os pontos identificados por (2), (3) e (5) correspondem à energia dos complexos ativados para as reações representadas.
Assinale a alternativa CORRETA.
I. o aumento da concentração dos reagentes diminui a velocidade da reação.
II. quanto maior a área de contato entre as fases dos reagentes, maior será a velocidade da reação.
III. quanto maior a energia de ativação, mais lenta será a reação.
IV. o aumento da temperatura do sistema diminui a velocidade da reação.
V. o uso de catalisador diminui a energia de ativação e, portanto, aumenta a velocidade de uma reação.
Assinale a alternativa CORRETA.
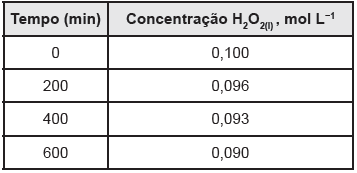
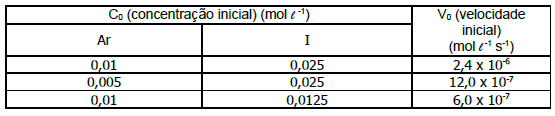
Com base nos dados da tabela, podemos concluir que, nos 200 min iniciais de reação, a velocidade de desaparecimento de H2 O2 (mol L−1 min−1) será de aproximadamente
Numa determinada condição experimental e com o catalisador adequado, ocorre uma reação, conforme representada no gráfico, que relaciona porcentagem do composto pelo tempo de reação.
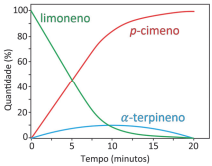
Uma representação adequada para esse processo é: