Questões de Vestibular de Química - Representação das transformações químicas
Foram encontradas 891 questões
Ano: 2023
Banca:
COMVEST - UNICAMP
Órgão:
UNICAMP
Prova:
COMVEST - UNICAMP - 2023 - UNICAMP - Vestibular - Conhecimentos Gerais - 1ª Fase |
Q2327088
Química
No início de 2023,
um grupo de pesquisadores estudou
o desenvolvimento
de uma poliamina
sólida contendo cobre, capaz de adsorver CO2
na fase
gasosa e em baixas
concentrações. A figura ao lado mostra
o esquema de adsorção com a representação do sólido:
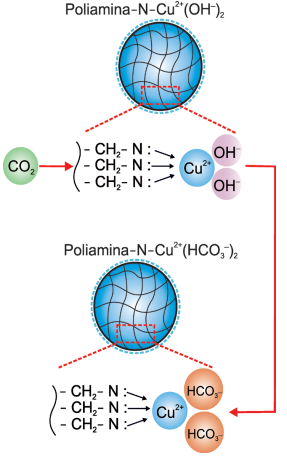
De acordo com os autores do estudo, 1 kg de poliamina contendo cobre é capaz de adsorver até 5 mols de CO2 , uma quantidade bem superior ao que se conhece até então. Com base nessas informações, pode-se concluir que a porcentagem em massa de cobre no sólido é cerca de

De acordo com os autores do estudo, 1 kg de poliamina contendo cobre é capaz de adsorver até 5 mols de CO2 , uma quantidade bem superior ao que se conhece até então. Com base nessas informações, pode-se concluir que a porcentagem em massa de cobre no sólido é cerca de
Ano: 2023
Banca:
COMVEST - UNICAMP
Órgão:
UNICAMP
Prova:
COMVEST - UNICAMP - 2023 - UNICAMP - Vestibular - Conhecimentos Gerais - 1ª Fase |
Q2327084
Química
Texto associado
Texto 1
A OMS (Organização Mundial de Saúde) recomenda que a ingestão de açúcares livres esteja abaixo de 5% da ingestão total
de energia diária para o nosso organismo. Como alternativa aos
açúcares livres, tem-se intensificado o uso de adoçantes não
nutritivos, como, por exemplo, sacarina, sucralose, stevia e aspartame. A própria OMS atualmente recomenda que adoçantes
não sejam utilizados para controlar a massa corporal, pois não
oferecem benefício na redução da gordura corporal. Uma bebida muito consumida no cotidiano, o refrigerante, apresenta
esses dois aspectos para os quais a OMS chama atenção: os
comuns têm cerca de 11 g de açúcar por 100 mL e os diets
contêm adoçantes não nutritivos.
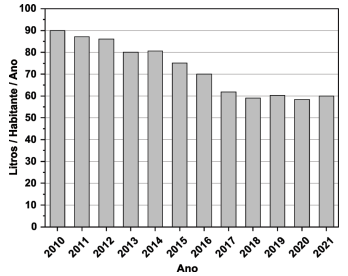
O gráfico a seguir apresenta o consumo médio de refrigerante
por habitante por ano, no período de 2010 a 2021, no Brasil.
Dados:
i) ingestão total de energia diária para adultos: 8400 kJ (recomendação da OMS).
ii) energia por grama de açúcar: 16,5 kJ.
De acordo com as informações do gráfico e do texto 1, pode-se afirmar que a média de consumo diário de açúcar, por habitante, para cada ano, devido somente à ingestão de refrigerante,

Dados:
i) ingestão total de energia diária para adultos: 8400 kJ (recomendação da OMS).
ii) energia por grama de açúcar: 16,5 kJ.
De acordo com as informações do gráfico e do texto 1, pode-se afirmar que a média de consumo diário de açúcar, por habitante, para cada ano, devido somente à ingestão de refrigerante,
Ano: 2023
Banca:
UERJ
Órgão:
UERJ
Prova:
UERJ - 2023 - UERJ - Vestibular Estadual 2024 – 1º Exame de Qualificação |
Q2182201
Química
Observe a equação química que representa a hidrólise do carbeto de cálcio.
CaC2 (s) + 2 H2 O (l) → Ca(OH)2 (aq) + C2 H2 (g)
O nome do composto orgânico obtido nessa reação é:
CaC2 (s) + 2 H2 O (l) → Ca(OH)2 (aq) + C2 H2 (g)
O nome do composto orgânico obtido nessa reação é:
Ano: 2022
Banca:
CEV-URCA
Órgão:
URCA
Prova:
CEV-URCA - 2022 - URCA - PROVA I: Física, Matemática, Química e Biologia |
Q2092943
Química
(URCA/2022.2) Marque a opção que correlaciona corretamente o nome do composto químico com a respectiva
fórmula molecular:
Ano: 2023
Banca:
PUC - RS
Órgão:
PUC - RS
Provas:
PUC - RS - 2022 - PUC - RS - Vestibular - Primeiro Semestre - Medicina
|
PUC - RS - 2023 - PUC - RS - Vestibular - Medicina |
Q2092741
Química
O clorofórmio (CHCl3) foi introduzido como anestésico em procedimentos cirúrgicos no século XIX, na
Inglaterra. Entretanto, o seu uso foi gradativamente
abandonado devido ao seu alto grau de toxicidade,
sendo substituído por substâncias anestésicas mais
adequadas. O clorofórmio pode ser preparado pela
reação de metano com cloro:
CH4(g) + 3 Cl2(g) → CHCl3(l) + 3 HCl(g)
A quantidade de cloro, em gramas, necessária para produzir 1,5 mol de clorofórmio é
CH4(g) + 3 Cl2(g) → CHCl3(l) + 3 HCl(g)
A quantidade de cloro, em gramas, necessária para produzir 1,5 mol de clorofórmio é