Questões Militares Sobre química para ita
Foram encontradas 226 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
II. A nitrificação é um processo de duas etapas no qual a amônia é convertida em nitrato por bactérias no solo: primeiro a amônia é oxidada a nitrito e, em seguida, o nitrito é oxidado a nitrato.
III. A desnitrificação é o processo pelo qual o nitrato é convertido novamente em nitrogênio atmosférico por bactérias desnitrificantes, processo que ocorre preferencialmente em condições de alto teor de oxigênio.
IV. As plantas contribuem para o ciclo do nitrogênio fixando o nitrogênio atmosférico por meio de relações simbióticas com bactérias fixadoras de nitrogênio.
V. O ciclo do nitrogênio consiste em várias etapas interconectadas, tais como: fixação, nitrificação, desnitrificação e amonificação.
Das afirmações acima, estão CORRETAS
II. Em uma mistura de octano e oxigênio, o combustível representa aproximadamente 78% da massa total.
III. A variação de temperatura da reação de combustível e oxigênio (por mol de combustível) é igual à variação de temperatura da reação de combustível e ar atmosférico (por mol de combustível).
IV. A entalpia molar de combustão de uma mistura de combustível e oxigênio é igual à entalpia molar de combustão de uma mistura de combustível e ar atmosférico. Assinale a opção que contém as afirmações CORRETAS.

I. A adição de um soluto não volátil a um solvente puro, em uma dada temperatura constante, sempre provoca uma diminuição na pressão de vapor.
II. A pressão de vapor de uma solução formada por dois líquidos voláteis é sempre menor que a pressão de vapor dos líquidos puros a uma mesma temperatura.
III. O valor absoluto do abaixamento no ponto de congelamento de uma solução é menor se o soluto dimeriza parcialmente no solvente, comparado ao sistema nas mesmas condições em que não há a dimerização do soluto.
IV. A pressão osmótica é a pressão exercida pelas moléculas de soluto numa membrana semipermeável.
V. Uma mistura formada por duas substâncias nunca solidifica inteiramente em uma única temperatura.
Assinale a opção que contém a(s) afirmação(ões) CORRETA(S):

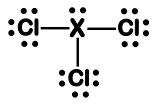
I. A molécula adota uma estrutura trigonal plana, com ângulo de ligação Cl-X-Cl maior ou igual a 120°.
II. A molécula adota uma estrutura tetraédrica, com ângulo de ligação Cl-X-Cl maior que 109,5°.
III. O átomo “X” pode ser o nitrogênio, preservando a geometria molecular. IV. O átomo “X” pode ser o boro, preservando a geometria molecular.
Assinale a opção que contém a(s) afirmação(ões) CORRETA(S):