Questões Militares de Química - Sistemas Homogêneos: Equilíbrio Químico na Água: pH e pOH, Indicadores Ácido-Base, Solução Tampão.
Foram encontradas 101 questões
Considerando que: - a solução básica foi parcialmente neutralizada pela solução do ácido; - o ácido clorídrico é um ácido forte (α=100%); - o hidróxido de sódio é uma base forte (α=100%).
O pH da mistura resultante dessa reação de neutralização é
Dado: log 4 = 0,60
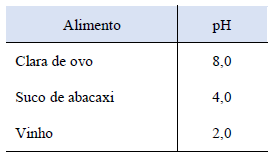
Com base nas informações da tabela abaixo, assinale a alternativa CORRETA.
Em um experimento de química, um estudante colocou em um recipiente 500 mL de uma solução aquosa de hidróxido de sódio (NaOH) em uma chapa de aquecimento. O pOH da solução antes do aquecimento era igual a 2. Após um tempo, considerando que se evaporou apenas água, o pOH da solução se reduziu à metade.
Nessas condições, é correto afirmar que o volume, em mililitros, da solução que permaneceu no recipiente ao fim do experimento é igual a
Considere a seguinte substância:

Com relação à reação abaixo, considerando a tabela acima e o pH da água igual a 7,00, assinale a opção correta.
CH3NH2(aq) + H2O(I) ⇄ CH3NH+3(aq) + OH-(aq)