Questões Militares de Química - Sistemas Homogêneos: Equilíbrio Químico na Água: pH e pOH, Indicadores Ácido-Base, Solução Tampão.
Foram encontradas 101 questões
Q2280185
Química
Considere 1 L de solução aquosa preparada por meio da adição de 1 mol de
um ácido monoprótico hipotético, 1 mol de sua base conjugada e 0,82 mol de uma base
forte. Sabendo que a constante de ionização do ácido é igual a 10-4, assinale a alternativa
que melhor representa o pH da solução resultante.
Ano: 2023
Banca:
VUNESP
Órgão:
EsFCEx
Prova:
VUNESP - 2023 - EsFCEx - Oficial - Magistério em Química |
Q2260527
Química
A dissolução em água de um comprimido antiácido efervescente forma alguns equilíbrios químicos, entre eles,
o sistema carbonato/bicarbonato representado a seguir:
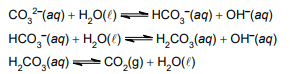
A solução tampão formada nesse sistema envolve o par conjugado ácido-base, nessa ordem:
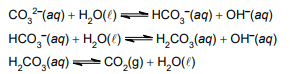
A solução tampão formada nesse sistema envolve o par conjugado ácido-base, nessa ordem:
Q2069043
Química
A escala de pH auxilia na manutenção da vida de muitos
sistemas. As águas de rios e mares, o sangue, o suco
gástrico, a qualidade da água potável, entre outros.
Assim, podemos controlar a acidez, a basicidade
e a neutralidade de sistemas, de acordo com as
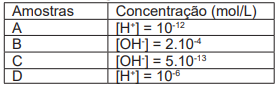
necessidades dos seres vivos. A tabela a seguir fornece
a concentração hidrogeniônica ou hidroxiliônica a 25°C,
em mol/L, de algumas amostras de soluções:
Tabela. Dados de amostras de acordo com suas concentrações hidrogeniônicas e hidroxiliônicas.
Use: log2= 0,3; log5= 0,7 (aproximações)
De acordo com os dados presentes na tabela, assinale a alternativa correta, quanto à acidez, à neutralidade ou à basicidade das amostras A, B, C e D.
Tabela. Dados de amostras de acordo com suas concentrações hidrogeniônicas e hidroxiliônicas.

Use: log2= 0,3; log5= 0,7 (aproximações)
De acordo com os dados presentes na tabela, assinale a alternativa correta, quanto à acidez, à neutralidade ou à basicidade das amostras A, B, C e D.
Q2024785
Química
A biodegradação da matéria orgânica produz substâncias húmicas, nas quais os principais componentes são os
ácidos húmicos. Estes correspondem a diversas estruturas complexas, que possuem na maioria substituintes
fenólicos (pKa = 8) e carboxílicos (pKa = 4). Além de alterar o pH do meio, também são capazes de se ligar a íons
metálicos formando coloides. Sobre esse tema, considere as seguintes afirmativas:
1. A presença de substâncias húmicas torna o pH menor que 7. 2. A presença de substâncias húmicas ligadas a íons metálicos é detectada pelo turvamento do meio. 3. O valor medido de pH 6 em uma amostra indica que praticamente todos os substituintes fenólicos estão protonados, enquanto que os substituintes carboxílicos estão desprotonados. 4. O valor medido de pH 4 em uma amostra indica que 50% dos substituintes carboxílicos estão protonados.
Assinale a alternativa correta.
1. A presença de substâncias húmicas torna o pH menor que 7. 2. A presença de substâncias húmicas ligadas a íons metálicos é detectada pelo turvamento do meio. 3. O valor medido de pH 6 em uma amostra indica que praticamente todos os substituintes fenólicos estão protonados, enquanto que os substituintes carboxílicos estão desprotonados. 4. O valor medido de pH 4 em uma amostra indica que 50% dos substituintes carboxílicos estão protonados.
Assinale a alternativa correta.
Q2015284
Química
Num experimento, foi montada a aparelhagem mostrada na figura ao lado.
Um tubo contendo 20 mL de ar está imerso na água da cuba. Pode-se
considerar que a composição do ar é 80% de N2(g) e 20% de O2(g). O NO(g)
formado no gerador passa pela mangueira até chegar ao tubo imerso na
água, como ilustrado.
Deixou-se o NO(g) borbulhar até que fossem acrescidos ao tubo 4 mL desse gás. Após cessar o fluxo de NO(g), o tubo foi mantido imerso na posição vertical, de modo que seu volume pudesse variar, mantendo a pressão em seu interior igual à pressão exterior, mas sem escape de gás. Após certo tempo, o gás dentro do tubo adquire cor castanha, em função da seguinte reação:
2 NO(g) + O2 (g) →2NO2 (g)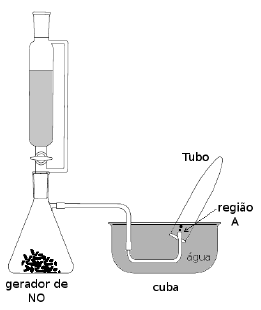
A respeito desse experimento, identifique as afirmativas abaixo como verdadeiras (V) ou falsas (F):
( ) O NO(g) é reagente limitante da reação.
( ) Em relação à condição imediata depois de cessado o fluxo, o volume de gás dentro do tubo irá diminuir após o gás ficar castanho.
( ) Em relação à condição imediata depois de cessado o fluxo, a pressão parcial de N2(g) dentro do tubo irá aumentar após o gás ficar castanho.
( ) O valor de pH da água na região A (dentro do tubo) irá diminuir após o gás se tornar castanho.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.
Deixou-se o NO(g) borbulhar até que fossem acrescidos ao tubo 4 mL desse gás. Após cessar o fluxo de NO(g), o tubo foi mantido imerso na posição vertical, de modo que seu volume pudesse variar, mantendo a pressão em seu interior igual à pressão exterior, mas sem escape de gás. Após certo tempo, o gás dentro do tubo adquire cor castanha, em função da seguinte reação:
2 NO(g) + O2 (g) →2NO2 (g)

A respeito desse experimento, identifique as afirmativas abaixo como verdadeiras (V) ou falsas (F):
( ) O NO(g) é reagente limitante da reação.
( ) Em relação à condição imediata depois de cessado o fluxo, o volume de gás dentro do tubo irá diminuir após o gás ficar castanho.
( ) Em relação à condição imediata depois de cessado o fluxo, a pressão parcial de N2(g) dentro do tubo irá aumentar após o gás ficar castanho.
( ) O valor de pH da água na região A (dentro do tubo) irá diminuir após o gás se tornar castanho.
Assinale a alternativa que apresenta a sequência correta, de cima para baixo.