Questões Militares de Química - Sistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores.
Foram encontradas 57 questões
Ano: 2012
Banca:
Exército
Órgão:
EsPCEx
Prova:
Exército - 2012 - EsPCEx - Cadete do Exército - 1° Dia |
Q615962
Química
Considere a seguinte reação química em equilíbrio num sistema fechado a uma temperatura
constante:

A respeito dessa reação, são feitas as seguintes afirmações:
I – a reação direta trata-se de um processo exotérmico;
II – o denominador da expressão da constante de equilíbrio em termos de concentração molar (Kc) é igual a [H2O]·[C];
III – se for adicionado mais monóxido de carbono (CO(g)) ao meio reacional, o equilíbrio será deslocado para a esquerda, no sentido dos reagentes;
IV – o aumento na pressão total sobre esse sistema não provoca deslocamento de equilíbrio.
Das afirmações feitas, utilizando os dados acima, está(ão) correta(s):

A respeito dessa reação, são feitas as seguintes afirmações:
I – a reação direta trata-se de um processo exotérmico;
II – o denominador da expressão da constante de equilíbrio em termos de concentração molar (Kc) é igual a [H2O]·[C];
III – se for adicionado mais monóxido de carbono (CO(g)) ao meio reacional, o equilíbrio será deslocado para a esquerda, no sentido dos reagentes;
IV – o aumento na pressão total sobre esse sistema não provoca deslocamento de equilíbrio.
Das afirmações feitas, utilizando os dados acima, está(ão) correta(s):
Ano: 2010
Banca:
FUNDEP (Gestão de Concursos)
Órgão:
CBM-MG
Prova:
FUNDEP (Gestão de Concursos) - 2010 - CBM-MG - Aspirante do Corpo de Bombeiro |
Q608776
Química
O tratamento de água de piscina envolve várias etapas. Uma delas é feita adicionando
hipoclorito de sódio que, ao entrar em contato com a água, sofre hidrólise e gera o
equilíbrio:
NaCℓO (aq) + H2O (l) HCℓO (aq) + Na+ (aq) + OH -(aq)
HCℓO (aq) + Na+ (aq) + OH -(aq)
Nesse equilíbrio, o ácido hipocloroso consegue atravessar as paredes celulares de bactérias e reagir com outras moléculas proteicas existentes dentro desses microorganismos. Desse modo, esse ácido atua como desinfetante, germicida e bactericida.
Analisando a equação do equilíbrio e a ação do ácido hipocloroso, é CORRETO afirmar que
NaCℓO (aq) + H2O (l)
 HCℓO (aq) + Na+ (aq) + OH -(aq)
HCℓO (aq) + Na+ (aq) + OH -(aq)
Nesse equilíbrio, o ácido hipocloroso consegue atravessar as paredes celulares de bactérias e reagir com outras moléculas proteicas existentes dentro desses microorganismos. Desse modo, esse ácido atua como desinfetante, germicida e bactericida.
Analisando a equação do equilíbrio e a ação do ácido hipocloroso, é CORRETO afirmar que
Ano: 2016
Banca:
CONSULPLAN
Órgão:
CBM-PA
Prova:
CONSULPLAN - 2016 - CBM-PA - Aspirante do Corpo de Bombeiro |
Q608642
Química
O sangue é vital para o funcionamento do organismo. Para que as trocas gasosas ocorram normalmente, o sangue deve estar tamponado com pH em torno de 7,4. O principal sistema tampão usado para controlar o pH no sangue é o sistema tampão ácido carbônico‐bicarbonato.
H+ (aq) + HCO– 3(aq)↔ H2CO3(aq) ↔ H2O(l) + CO2(g)
A regulagem do pH do plasma sanguíneo relaciona‐se diretamente ao transporte efetivo de O2 para os tecidos corpóreos. O oxigênio é carregado pela proteína hemoglobina encontrada nas células de glóbulos vermelhos. A hemoglobina (Hb) liga‐se reversivelmente tanto ao H+ quanto ao O2.
HbH+ + O2↔ HbO2 + H+
De acordo com as reações apresentadas, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Durante períodos de esforço vigoroso grandes quantidades de CO2 são produzidas pelo metabolismo, que desloca o equilíbrio para a direita, diminuindo o pH.
( ) Quando o sangue atinge os tecidos nos quais a concentração de O2 é baixa, o equilíbrio desloca‐se para a esquerda e O2 é liberado.
( ) Durante períodos de esforço vigoroso, à medida que O2 é consumido, o equilíbrio desloca‐se para a direita de acordo com o princípio de Le châtelier.
( ) A remoção de CO2 por exalação desloca o equilíbrio para a direita, consumindo íons H+ .
A sequência está correta em
H+ (aq) + HCO– 3(aq)↔ H2CO3(aq) ↔ H2O(l) + CO2(g)
A regulagem do pH do plasma sanguíneo relaciona‐se diretamente ao transporte efetivo de O2 para os tecidos corpóreos. O oxigênio é carregado pela proteína hemoglobina encontrada nas células de glóbulos vermelhos. A hemoglobina (Hb) liga‐se reversivelmente tanto ao H+ quanto ao O2.
HbH+ + O2↔ HbO2 + H+
De acordo com as reações apresentadas, marque V para as afirmativas verdadeiras e F para as falsas.
( ) Durante períodos de esforço vigoroso grandes quantidades de CO2 são produzidas pelo metabolismo, que desloca o equilíbrio para a direita, diminuindo o pH.
( ) Quando o sangue atinge os tecidos nos quais a concentração de O2 é baixa, o equilíbrio desloca‐se para a esquerda e O2 é liberado.
( ) Durante períodos de esforço vigoroso, à medida que O2 é consumido, o equilíbrio desloca‐se para a direita de acordo com o princípio de Le châtelier.
( ) A remoção de CO2 por exalação desloca o equilíbrio para a direita, consumindo íons H+ .
A sequência está correta em
Q603384
Química
O dióxido de nitrogênio, proveniente da queima de combustíveis fósseis, é uma das espécies que mais contribui para
o efeito da chuva ácida. A reação química que provoca a diminuição do pH da água da chuva é representada pelo
equilíbrio a seguir:
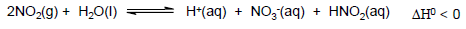
Num ensaio em laboratório, foram acondicionados num sistema fechado N2(g), O2(g), NO2(g) e vapor de água que está em equilíbrio com água líquida. A partir desses dados, considere as seguintes afirmações:
1. O aumento na pressão total do sistema tenderá a diminuir o pH da solução dentro do sistema.
2. Um aquecimento brando tenderá a aumentar o pH da solução dentro do sistema.
3. A adição de excesso de água líquida no sistema tenderá a deslocar o equilíbrio, diminuindo o pH da solução dentro do sistema.
4. A contribuição do ácido nitroso (HNO2) para o pH da solução dentro do sistema é desprezível.
Assinale a alternativa correta
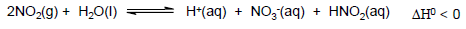
Num ensaio em laboratório, foram acondicionados num sistema fechado N2(g), O2(g), NO2(g) e vapor de água que está em equilíbrio com água líquida. A partir desses dados, considere as seguintes afirmações:
1. O aumento na pressão total do sistema tenderá a diminuir o pH da solução dentro do sistema.
2. Um aquecimento brando tenderá a aumentar o pH da solução dentro do sistema.
3. A adição de excesso de água líquida no sistema tenderá a deslocar o equilíbrio, diminuindo o pH da solução dentro do sistema.
4. A contribuição do ácido nitroso (HNO2) para o pH da solução dentro do sistema é desprezível.
Assinale a alternativa correta
Q591305
Química
Quantidades iguais de H2(g) e I2(g) foram colocadas em um frasco, com todo o sistema à temperatura T, resultando na pressão total de 1 bar. Verificou-se que houve a produção de HI(g), cuja
22,8 kPa. Assinale a alternativa que apresenta o valor que mais se aproxima do valor CORRETO da constante de equilíbrio desta reação.