Questões Militares de Química - Sistemas Homogêneos: Constantes: Kc e Kp. Deslocamento do Equilíbrio: Fatores.
Foram encontradas 57 questões
Constantes de equilíbrio de ácidos fracos a 25 oC

Com base nas informações fornecidas, qual dos sais indicados a seguir é o mais eficiente como solução neutralizante?
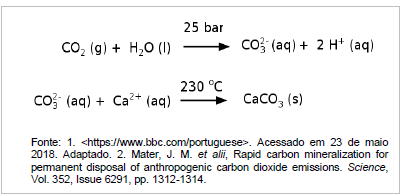
A remoção desse gás da atmosfera ocorre por:
O sulfito de sódio (Na2SO3 ) é um sal inorgânico muito utilizado como conservante de alimentos e na manufatura de papel. Um dos processos de produção do sulfito de sódio pode ser obtido mediante a seguinte equação na condição de equilíbrio químico.
Na2O(s) + SO2(g) ⇋ Na2SO3(s) ∆H < 0
Considerando que para a reação de produção em um processo industrial é desejável que se produza mais sulfito de sódio partindo de um sistema em equilíbrio, qual fator é adequado para tal processo?
Analise a seguinte reação.
2NO2(g) ⇄ N2O4(g) ΔH = -57,2 kJ/mol
Na reação acima, o equilíbrio se desloca para a esquerda
quando, considerando conjuntamente os efeitos da
compressão e temperatura sobre o sistema:
Dadas as seguintes equações que representam supostas reações químicas irreversíveis em meio aquoso e temperaturas moderadas:
I) 6 HBr + 2 Al → 2 AlBr3 + 3 H2
II) H2SO4 + BaCl2 → BaSO4 + 2 HCl
III) 2 KOH + NiSO4 → Ni(OH)2 + K2SO4
IV) 2 HBr + K2S → 2 KBr + H2S
V) BaCl2 + Na2CO3 → BaCO3 + 2 NaCl
Pode-se afirmar que a reação: