Laboratórios de química geram como subprodutos substâncias ...
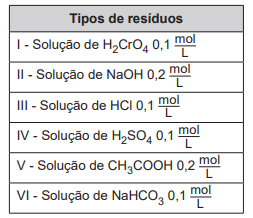
Qual combinação de resíduos poderá ser descartada na rede de esgotos?
- Gabarito Comentado (1)
- Aulas (19)
- Comentários (6)
- Estatísticas
- Cadernos
- Criar anotações
- Notificar Erro
Gabarito comentado
Confira o gabarito comentado por um dos nossos professores
Clique para visualizar este gabarito
Visualize o gabarito desta questão clicando no botão abaixo
Comentários
Veja os comentários dos nossos alunos
O H2SO4 tem 2 H- para neutralizar precisa do dobro de OH-, que apresenta no 0,2 mol no NaOH
Não pode ser a letra B pois fica desbalanceado com OH2- por conta da concentração
Bom a formação tem que ser neutra, livre de solventes inflamáveis e sem elementos tóxicos.
Neutra- AC forte com Base forte
AC frraco com base fraca
A INCORRETO, apresenta elemento tóxico
B INCORRETO, apesar de formar um sal neutro e não ter elemento tóxico, a concentração nao bate para realizar a equação. 0,2 NaOH + 0,1 HCl ---- NaCl + H2O. Assim, 0,2 Na somente formaria 0,1 de NaCl
C CORRETA diferente da letra b a concentração é proporcional
D INCORRETA ac. acetico + sal básico. ac acetico esta no vinagre e esse é um acido fraco
E INCORRETA ac + sal basico. ac acetico é um acido fraco
"Para o descarte na rede de esgoto, o resíduo deve ser neutro, livre de solventes inflamáveis e elementos tóxicos como Pb, Cr e Hg." Qual combinação de resíduos poderá ser descartada na rede de esgotos? II + IV. E como a proporção para neutralização é de H2 para OH2, assim, I +II tem resíduo com Cr, II +III tem excesso de base, V + VI e IV+VI tem excesso de acido
H2SO4 + 2NAOH > NA2SO4 + 2H20
Ác. Forte + Base Forte = caráter neutro
Minha base precisa fornecer duas hidroxilas para neutralizar o dois H+.
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo