Questões de Vestibular de Química - Sistemas Homogêneos: Equilíbrio Químico na Água: pH e pOH, Indicadores Ácido-Base, Solução Tampão.
Foram encontradas 330 questões
Ano: 2010
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2010 - UEFS - Vestibular - FÍSICA, QUÍMICA e BIOLOGIA |
Q1374125
Química
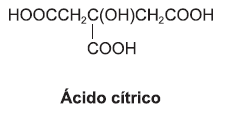
O ácido cítrico, responsável pela acidez das frutas cítricas, é utilizado como acidificante e flavorizante no processamento de alguns alimentos.
A partir dessas informações, é correto afirmar:
Ano: 2010
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2010 - UEFS - Vestibular - FÍSICA, QUÍMICA e BIOLOGIA |
Q1374124
Química
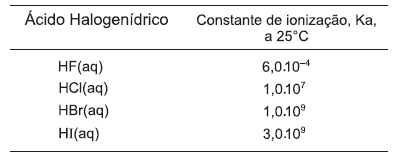
A tabela relaciona os valores da constante de ionização, Ka, dos ácidos halogenídricos.
A partir da análise dessa tabela, é correto afirmar:
Ano: 2010
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2010 - UEFS - Vestibular - FÍSICA, QUÍMICA e BIOLOGIA |
Q1374116
Química
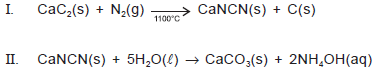
Quando carbeto de cálcio, CaC2, é aquecido em um forno elétrico, na presença de nitrogênio atmosférico, a 1100°C, dá origem à cianamida de cálcio, empregada largamente como fertilizante nitrogenado de ação lenta, pois leva alguns meses, no solo, para se hidrolisar de acordo com a equação química II. Como a cianamida de cálcio não é arrastada pelas chuvas, é um fertilizante melhor do que o nitrato de amônio, NH4NO3, e a ureia, CO(NH2)2.
Uma análise dessas informações permite afirmar:
Ano: 2009
Banca:
UEFS
Órgão:
UEFS
Prova:
UEFS - 2009 - UEFS - Vestibular - Física, Química e Biologia |
Q1372632
Química
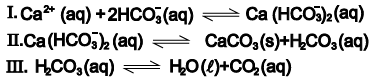
As algas zooxanthellae são também responsáveis pela intensa precipitação de carbonatos no esqueleto dos corais escleractíneos principais formadores dos recifes. Em pH próximo a 8,5, a maior parte do CO2 (aq) disponível na água do mar se encontra na forma de íons bicarbonato, HCO3- (aq). Devido à intensa radiação solar, os corais e os invertebrados que possuem algas simbiontes — sensíveis a pequenas alterações de temperatura — capturam ativamente íons de cálcio, Ca2+(aq), que reagem com íons bicarbonato.O bicarbonato de cálcio se decompõe em carbonato de cálcio, que se precipita sob forma de esqueleto, e ácido carbônico, H2CO3 (aq), usado na fotossíntese. Trata-se de um processo bioquímico muito eficiente, porém sujeito às alterações das concentrações de CO2 (g), na atmosfera.
Uma análise do processo bioquímico de formação de esqueleto de carbonato de cálcio dos corais escleractíneos referidos no texto e de acordo com as equações químicas I, II e III, permite afirmar:
Ano: 2019
Banca:
FAG
Órgão:
FAG
Provas:
FAG - 2019 - FAG - Vestibular - Segundo Semestre - Medicina
|
FAG - 2019 - FAG - Vestibular - Segundo Semestre |
Q1369817
Química
O leite de vaca possui um pH médio de 6,6. Em caso de mastite, ou seja, inflamação da glândula mamária
causada por bactérias, o pH torna-se alcalino. As bactérias acidificam o leite, mas o organismo do animal, para
compensar, libera substâncias alcalinas. Qual deve ser o valor do pH do leite de um animal com mastite?