Um experimento de cromatografia em camada fina, utilizando p...
Comentários
Veja os comentários dos nossos alunos
Em fase Normal (geralmente sílica): Substâncias apolares eluem mais rapidamente que substâncias polares, porque os compostos polares possuem maiores interações com a fase estacionária (polar).
Em fase reversa (-C2; -C8 e -C18): Substâncias polares eluem mais rapidamente que as apolares, porque os compostos apolares possuem maior interação com a fase estacionária (apolar).
Além disso, substâncias com maior peso molecular (e a mesma polaridade) eluem mais lentamente que os análogos menores (menores interações Van der Waals).
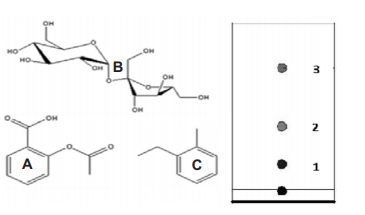
C é apolar e B é muito mais apolar que A. Logo, C é a mais retida, enquanto B é a menos retida.
ESTRUTURA A: polaridade intermediária, migra mais do que C e menos do que B.
ESTRUTURA B: maior número de hidroxilas, portanto, maior polaridade. Múltiplo grupos OH formam ligações de hidrogênio com a fase móvel (polar). Corre primeiro e mais rápido, por isso 3.
ESTRUTURA C: presença de anel aromático indica caráter apolar + baixa quantidade de grupos polares + predomínio de ligações C-H e C-C= estrutura menos polar. Portanto, fica mais retida na fase estacionária (Apolar), por isso, posição 1.
Clique para visualizar este comentário
Visualize os comentários desta questão clicando no botão abaixo