Questões de Concurso Público UFPA 2017 para Químico
Foram encontradas 6 questões
A constante de equilíbrio para a dissociação de um mol ácido monoprótico em 1 litro de água é aproximadamente 1x10-5 à temperatura de 25 ºC. Se a pressão é constante, o valor aproximado da variação na energia de Gibbs (kJ mol-1) para essa reação é de
DADOS:
Constante dos gases ideais = 8,31 J K-1 mol-1 Log10 e = 0,434
O Diagrama de Orbitais Moleculares (DOM) para o íon molecular H2 + pode ser obtido pela Combinação Linear de Orbitais Atômicos (CLOA) das funções de onda normalizadas que designam o orbital s de um átomo de hidrogênio a, representado como 1sa, com a função onda normalizada do átomo de hidrogênio b, representado como 1sb. Essas combinações lineares estão mostradas abaixo:

A ordem de ligação em H2 + é
Dado: 1H = 1s1.
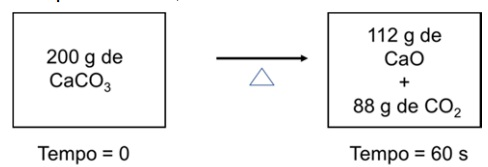
O acúmulo total de massa, em gramas, para a decomposição térmica do carbonato de cálcio em um sistema fechado, representado pelo esquema abaixo, é
Pode-se considerar que o processo Rasching de produção de hidrazina (N2H4), que envolve a oxidação de amônia, ocorre em três etapas consecutivas, representadas pelas equações químicas não balanceadas na sequência abaixo:
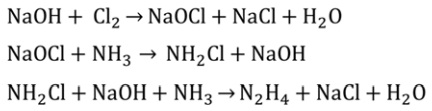
Assim, o número de mol de amônia necessários para a produção de dois mol de hidrazina é
A massa atômica relativa dos elementos é obtida pela determinação da média ponderada de seus isótopos. Dentre os elementos do grupo 14 da tabela periódica, mostrados abaixo, o que apresenta maior incerteza na sua massa atômica relativa é o
Elemento: C; Si; Ge; Sn; Pb
Massa Atômica relativa (u): 12,011; 28,086; 72,61(2); 118,71; 207,2