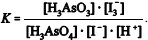Questões de Concurso Público FUB 2015 para Químico
Foram encontradas 120 questões
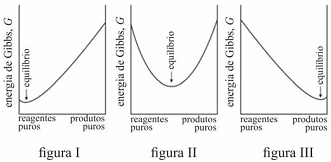
É possível prever, termodinamicamente, se os reagentes de uma mistura têm a tendência espontânea para se transformarem em produtos, se a composição, no equilíbrio, será modificada ao se alterarem as condições de um sistema, entre outros comportamentos termodinâmicos. Acerca de equilíbrio químico e considerando os gráficos representados nas figuras I, II e III, que mostram três situações de equilíbrio, julgue o item que se segue.
Em uma reação química, a variação da energia de Gibbs de
reação com a temperatura depende da entropia de reação. A
energia de Gibbs de uma reação que produz gás aumenta com
o aumento da temperatura.
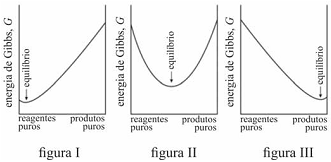
É possível prever, termodinamicamente, se os reagentes de uma mistura têm a tendência espontânea para se transformarem em produtos, se a composição, no equilíbrio, será modificada ao se alterarem as condições de um sistema, entre outros comportamentos termodinâmicos. Acerca de equilíbrio químico e considerando os gráficos representados nas figuras I, II e III, que mostram três situações de equilíbrio, julgue o item que se segue.
O critério termodinâmico para uma transformação espontânea, à temperatura e à pressão constantes, é que a variação da energia de Gibbs seja maior que zero.
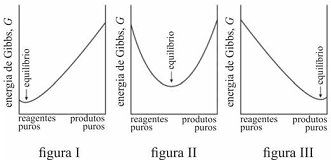
É possível prever, termodinamicamente, se os reagentes de uma mistura têm a tendência espontânea para se transformarem em produtos, se a composição, no equilíbrio, será modificada ao se alterarem as condições de um sistema, entre outros comportamentos termodinâmicos. Acerca de equilíbrio químico e considerando os gráficos representados nas figuras I, II e III, que mostram três situações de equilíbrio, julgue o item que se segue.
Na reação representada pelo gráfico da figura I, quantidades muito pequenas dos reagentes se convertem em produtos antes que G alcance seu valor mínimo e a reação se processe lentamente.
Considere que a reação química apresentada a seguir tenha ocorrido em meio aquoso, e que a velocidade dessa reação e a extensão na qual ela procede, para direita, podem ser prontamente avaliadas pela observação da cor vermelho-alaranjada do íon triiodeto I3- (os outros participantes da reação são incolores).
H3AsO4 + 3I- + 2H+ ↔ H3AsO3 + I-3 + H2O
Considerando essas informações, julgue o item subsecutivo.
Considerando a reação H3AsO3 + I-3 ↔ H3AsO4 + 3I- + 2H+ , é correto afirmar que, ao se adicionar 1 mmol de ácido arsenioso, H3AsO3, a 100 mL de uma solução, contendo 1 mmol de íon triiodeto, a solução produzida será incolor.
Considere que a reação química apresentada a seguir tenha ocorrido em meio aquoso, e que a velocidade dessa reação e a extensão na qual ela procede, para direita, podem ser prontamente avaliadas pela observação da cor vermelho-alaranjada do íon triiodeto I3- (os outros participantes da reação são incolores).
H3AsO4 + 3I- + 2H+ ↔ H3AsO3 + I-3 + H2O
Considerando essas informações, julgue o item subsecutivo.
A constante de equilíbrio da reação apresentada pode ser corretamente expressa como