Questões de Química - Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess. para Concurso
Foram encontradas 355 questões
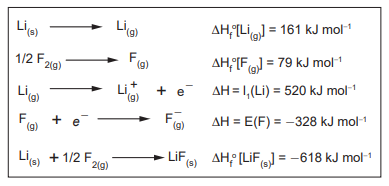
Nesse contexto, o valor aproximado da entalpia de rede (ΔHrede) para o LiF(s), em kJ mol-1 , é
CH4(g) + 2O2(g) → CO2(g) + 2 H2O(l)
Dados:
Calores de Formação:
• H2O (l): ΔHf = - 68 kcal/mol • CO2 (g): ΔHf = - 94 kcal/mol • CH4(g): ΔHf = - 18 kcal/mol
De acordo com os dados dos calores de formação acima, assinale a alternativa que apresenta a entalpia (ΔH) da reação.

Internet:<www.tabelaperiodica.org>
Acerca da espectroscopia de absorção molecular no ultravioleta e no visível, julgue o item.
À medida que o número de moléculas capazes de absorver luz de um determinado comprimento de onda aumenta, a extensão dessa absorção diminui, de acordo com a Lei de Lambert‑Beer expressa pela equação a seguir.
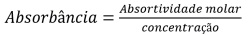

Internet:<www.tabelaperiodica.org>
Em relação à termodinâmica química, julgue o item.
A entalpia não é uma função de estado, o que significa
que sua variação depende do caminho percorrido, e
não apenas dos estados inicial e final.

Internet:<www.tabelaperiodica.org>
Em relação à termodinâmica química, julgue o item.
Em uma reação química conduzida à pressão
constante, se o sistema liberar 45 kJ.mol‑1 de calor (Q)
e realizar 20 kJ.mol‑1 de trabalho de expansão (W), a
variação da entalpia será de ‑45 kJ.mol‑1.