Questões de Química - Termoquímica: Energia Calorífica, Calor de reação, Entalpia, Equações e Lei de Hess. para Concurso
Foram encontradas 102 questões
Considere os dados termoquímicos:
B2H6(g) + 3 O2(g) → B2O3(s) + 3 H2O(g) ΔHo= -1941 kJ mol–1 2 B(s) + 3/2 O2(g) → B2O3(s) ΔHo= -2368 kJ mol–1 H2(g) + 1/2 O2(g) → H2O(g) ΔHo= -241,8 kJ mol–1
A entalpia padrão de formação do diborano (em kJ mol–1) é
A2 + B2 → 2 AB
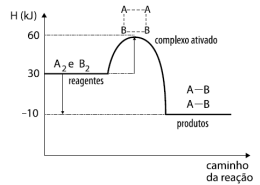
Disponível em: i_662d64349cafcb5b_html_55011cd1.png (463×350) (quimicaevestibular.com.br). Acesso em 27 de Julho de 2021.
Com relação ao gráfico acima, temos as seguintes afirmativas: I. A reação absorve calor; II. A energia de ativação da reação é 60 KJ; III. O valor da entalpia da reação (∆H) é de -40 KJ; IV. Ao colocarmos um catalisador na reação, diminuímos a sua entalpia (∆H), tornando-a mais rápida.
Estão corretas as afirmativas:
Atenção: a Tabela abaixo deve ser usada como apoio para responder a questão de Química.
A tabela a seguir contém algumas dessas substâncias e suas respectivas entalpias de combustão (ΔHc0):
Substância Fórmula ΔHc 0 (kJ.mol-1 )
Metano CH4 –890
Butano C4H10 –2878
Octano C8H18 –5471
Metanol CH3OH –726
Etanol C2H5OH –1368
A substância que libera a maior quantidade de energia por grama de combustível é o
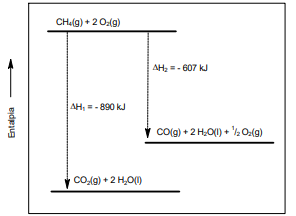
A partir dos dados apresentados, analise as afirmações:
I. Os valores de ΔH1 e ΔH2 indicam processos exotérmicos.
II. A energia envolvida na combustão parcial de 1 mol de metano é 890 kJ.
III. A combustão de 5 mols de monóxido de carbono (CO) libera 1415 kJ.
Está correto apenas o que se afirma em

Considerando essas informações e os diversos aspectos a elas relacionados, julgue o item.
Conclui-se que a conversão da hematita para Fe(s) é
favorecida em temperaturas abaixo de 623 K.