Questões de Química - Soluções: características, tipos de concentração, diluição, mistura, titulação e soluções coloidais. para Concurso
Foram encontradas 270 questões
Q2293511
Química
Identifique o processo que pode ocasionar a contaminação de um precipitado pela
incorporação de substâncias solúveis impuras que são arrastadas da solução durante a
formação do precipitado:
Q2284075
Química
Investigações da Polícia Federal revelaram que garimpeiros usaram cianeto para extrair ouro em um garimpo ilegal em
terras da União. O íon cianeto possui elevada toxicidade e, se despejado no ambiente, é devastador, podendo levar à
morte todos os seres vivos num raio de quilômetros. O cianeto de sódio é utilizado para dissolver ouro incrustado em
minérios, num processo com eficiência próxima a 100%, segundo a equação:
4 Au(minério) + 8 NaCN(aq) + O2(g) + 2 H2O(l) → 4 Na[Au(CN)2](aq) + 4 NaOH(aq)
A espécie química solúvel [Au(CN)2]− é posteriormente imobilizada sobre carvão ativado, e o ouro é recuperado por redução eletroquímica:
[Au(CN)2]−(aq) + e− → Au(s) + 2 CN−(aq)
Dados: Massa molar (g mol−1): Au = 197, NaCN = 49.
Considerando a estequiometria das reações, qual é a massa de ouro que se espera extrair, utilizando-se 1 kg de cianeto de sódio?
4 Au(minério) + 8 NaCN(aq) + O2(g) + 2 H2O(l) → 4 Na[Au(CN)2](aq) + 4 NaOH(aq)
A espécie química solúvel [Au(CN)2]− é posteriormente imobilizada sobre carvão ativado, e o ouro é recuperado por redução eletroquímica:
[Au(CN)2]−(aq) + e− → Au(s) + 2 CN−(aq)
Dados: Massa molar (g mol−1): Au = 197, NaCN = 49.
Considerando a estequiometria das reações, qual é a massa de ouro que se espera extrair, utilizando-se 1 kg de cianeto de sódio?
Ano: 2023
Banca:
PR-4 UFRJ
Órgão:
UFRJ
Prova:
PR-4 UFRJ - 2023 - UFRJ - Técnico de Laboratório - Química |
Q2272668
Química
Para determinar a pureza de uma amostra de
Na3
PO3
, um químico dissolveu 0,15 g de Na3
PO3
em 25 mL de água destilada. Em seguida, gotejou a solução do Na3
PO3
em uma solução contendo 50 mL de uma solução 3,0% (m/v) de cloreto
de mercúrio (II), 20 mL de uma solução de 10%
(m/v) de acetato de sódio e 5,0 mL de ácido acético. Após a oxidação do PO3
3- em PO4
3-, o químico
observou a formação de 0,39 g de Hg2
Cl2
. Assinale a alternativa que indica a pureza correta do
Na3
PO3
.
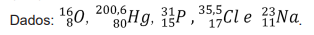
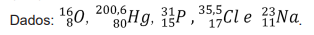
Ano: 2023
Banca:
FEPESE
Órgão:
Companhia Águas de Joinville
Prova:
FEPESE - 2023 - Companhia Águas de Joinville - Analista Químico |
Q2265700
Química
Em uma análise volumétrica para neutralização de
60 mL de solução de hidróxido de sódio (NaOH) com
concentração de 1,0 mol/L utilizou-se uma solução de
ácido sulfúrico (H2SO4) com concentração de 0,6 mol/L.
Qual o volume de solução de ácido necessário para essa neutralização?
Qual o volume de solução de ácido necessário para essa neutralização?
Ano: 2023
Banca:
FEPESE
Órgão:
Companhia Águas de Joinville
Prova:
FEPESE - 2023 - Companhia Águas de Joinville - Técnico em Sistemas de Saneamento - Químico |
Q2264972
Química
Em uma titulação de 1,125 g de solução de ácido
nítrico foram gastos 100 mL de uma solução de hidróxido de potássio.
Qual a concentração da solução de hidróxido de potássio para neutralizar completamente o ácido?
Considere a massa molar do HNO3 igual a 63 g/mol e a massa molar do KOH igual a 56 g/mol.
Qual a concentração da solução de hidróxido de potássio para neutralizar completamente o ácido?
Considere a massa molar do HNO3 igual a 63 g/mol e a massa molar do KOH igual a 56 g/mol.