Questões de Química - Equilíbrio Químico para Concurso
Foram encontradas 269 questões
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210810
Química
Um professor queria fazer uma prática de laboratório e necessitava de 10 mL de éster. Como não tinha o éster
no laboratório, ele pediu ao técnico que preparasse uma mistura de álcool, ácido e água. O técnico misturou
1,0 mol de metanol (C2H5OH), 1,0 mol de ácido etanóico (CH3COOH) e 1,0 mol de água. Depois de 30 horas a
25 °C, ao analisar a mistura, observou-se que, ao atingir o equilíbrio, 50% do ácido estava esterificado. Na
análise, o técnico descobriu que A CONSTANTE DE EQUILÍBRIO da reação é:
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210804
Química
A autoionização da água é um processo muito importante, pois dependendo da sua posição de equilíbrio
químico, define-se a acidez (ou alcalinidade) das soluções aquosas. Através de experimentos de condutividade
elétrica da água pura e da sua condutância específica, é possível determinar o grau de ionização da água e,
posteriormente, a constante de equilíbrio, Kw, da reação de autoionização. A 25 °C, o valor de Kw é 1,00 x 10-14
.
Por outro lado, para a água pura, a 37 °C, o grau de ionização é 73% maior, tendo em vista que a autoionização
da água é endotérmica. Vale ressaltar que nesta variação de temperatura a concentração molar da água é
praticamente invariável.
Diante das informações e a partir dos seus conhecimentos, assinale a opção que mostra aproximadamente O VALOR DO pOH de uma solução de pH 8,50, a 37 °C:
Dados: densidade da água = 1000 g/L; massa molar da água = 18 g/mol; log(1,73) = 0,24; log(3) = 0,48.
Diante das informações e a partir dos seus conhecimentos, assinale a opção que mostra aproximadamente O VALOR DO pOH de uma solução de pH 8,50, a 37 °C:
Dados: densidade da água = 1000 g/L; massa molar da água = 18 g/mol; log(1,73) = 0,24; log(3) = 0,48.
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210802
Química
Um certo ácido orgânico, Y, encontra-se parcialmente na forma de dímeros (reação: 2Y(g) ⇌ Y2(g) ), quando em
fase de vapor. Na temperatura de 298 K e sob pressão total de 0,200 atm, este ácido tem um grau de
dimerização de 90%.
Diante dessas informações, assinale a opção que mostra O VALOR DA CONSTANTE DE EQUILÍBRIO, Kp, para a reação de dimerização e a afirmação CORRETA que expressa a influência da pressão (FAVORECE OU DESFAVORECE) na dimerização:
Diante dessas informações, assinale a opção que mostra O VALOR DA CONSTANTE DE EQUILÍBRIO, Kp, para a reação de dimerização e a afirmação CORRETA que expressa a influência da pressão (FAVORECE OU DESFAVORECE) na dimerização:
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210796
Química
O hidróxido de zinco, Zn(OH)2, por ser um importante precursor do óxido de zinco, ZnO, tem diversas aplicações
em diferentes áreas. Algumas das principais incluem a produção de cosméticos e protetores solares e a
vulcanização da borracha. Esse hidróxido é insolúvel em água, com constante produto de solubilidade, Kps, igual
a 1,2 x 10-17
, a 25 °C.
Diante das informações, assinale a opção que mostra o valor do pH (após o equilíbrio) de uma solução em que são adicionados 0,01 mol/L de Zn2+ e 0,02 mol/L de OH- , a 25 °C: Dados eventualmente necessários: Kw (H2O), a 25 °C = 1,00 x 10-14; (3)1/3 = 1,44; log (1,44) = 0,16; log (2,88) = 0,46; (6)1/2 = 2,45; log (2,45) = 0,39; log (4,9) = 0,69.
Diante das informações, assinale a opção que mostra o valor do pH (após o equilíbrio) de uma solução em que são adicionados 0,01 mol/L de Zn2+ e 0,02 mol/L de OH- , a 25 °C: Dados eventualmente necessários: Kw (H2O), a 25 °C = 1,00 x 10-14; (3)1/3 = 1,44; log (1,44) = 0,16; log (2,88) = 0,46; (6)1/2 = 2,45; log (2,45) = 0,39; log (4,9) = 0,69.
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210795
Química
O termo “superácido” é usado para descrever os ácidos mais fortes do que o ácido sulfúrico, um dos ácidos
comuns mais fortes. George Andrew Olah (1927 - 2017), um químico húngaro-estadunidense, ganhou o Prêmio
Nobel de Química em 1994, com a aplicação de superácidos ao estudo de carbocátions. A água é um solvente
incapaz de distinguir os superácidos do ácido sulfúrico, uma vez que ela apresenta o chamado “efeito nivelador”.
Portanto, na quantificação da acidez dos superácidos é comum o uso da função de acidez de Hammett, H0, que
é definida matematicamente como:
H0 = pKa(BH+) - log [BH+] / [B]
onde B é um indicador básico, BH+ é o ácido conjugado desse indicador e pKa(BH+) é a constante de acidez deste último. Quando o indicador é nitroanilina (C6H6N2O2), experimentos realizados para ácidos puros nas mesmas condições, permitem construir a tabela abaixo:
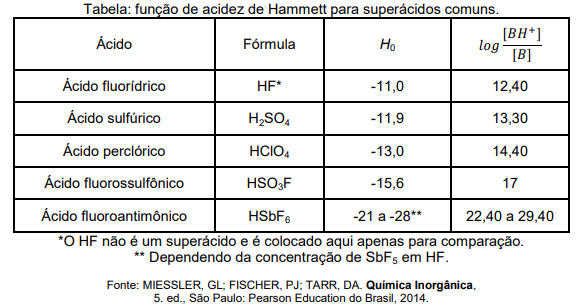
Diante dessas informações, assinale a opção que mostra a ÚNICA reação termodinamicamente espontânea entre pares das substâncias citadas acima:
H0 = pKa(BH+) - log [BH+] / [B]
onde B é um indicador básico, BH+ é o ácido conjugado desse indicador e pKa(BH+) é a constante de acidez deste último. Quando o indicador é nitroanilina (C6H6N2O2), experimentos realizados para ácidos puros nas mesmas condições, permitem construir a tabela abaixo:

Diante dessas informações, assinale a opção que mostra a ÚNICA reação termodinamicamente espontânea entre pares das substâncias citadas acima: