Questões Militares Para ita
Foram encontradas 1.149 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Q1901491
Química
Texto associado

Constantes
Constante de Avogadro (NA) = 6,02 x 1023 mol-1
Constante de Faraday (F) = 9,65 x 104 C.mol-1 = 9,65 x104 A.s.mol-1 = 9,65 x 104 J.V-1mol-1
Carga elementar = 1,60 x 10-19 C
Constante dos gases (R) = 8,21 x 10-2 atm.L.K-1.mol-1 = 8,31 J.K-1.mol-1 = 1,98 cal.K-1.mol-1
Constante de Planck (h) = 6,63 x 10-34 J.s
Velocidade da luz no vácuo = 3,0 x 108 m.s-1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 x 105 N.m-2 = 1,01325 bar
Energia: 1 J = 1 N.m = 1 kg.m2.s-2 = 6,24 x 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 ºC e 1 atm
Condições ambientes: 25 ºC e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol.L-1 (rigorosamente: atividade unitária das
espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol.L-1
ln X = 2,3 log X
EPH = eletrodo padrão de hidrogênio
Massas Molares

Assinale a opção que apresenta a sequência que melhor descreve o ciclo de ações envolvidas no
método científico (hipotético - dedutivo):
Q1901490
Química
Texto associado

Constantes
Constante de Avogadro (NA) = 6,02 x 1023 mol-1
Constante de Faraday (F) = 9,65 x 104 C.mol-1 = 9,65 x104 A.s.mol-1 = 9,65 x 104 J.V-1mol-1
Carga elementar = 1,60 x 10-19 C
Constante dos gases (R) = 8,21 x 10-2 atm.L.K-1.mol-1 = 8,31 J.K-1.mol-1 = 1,98 cal.K-1.mol-1
Constante de Planck (h) = 6,63 x 10-34 J.s
Velocidade da luz no vácuo = 3,0 x 108 m.s-1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 x 105 N.m-2 = 1,01325 bar
Energia: 1 J = 1 N.m = 1 kg.m2.s-2 = 6,24 x 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 ºC e 1 atm
Condições ambientes: 25 ºC e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol.L-1 (rigorosamente: atividade unitária das
espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol.L-1
ln X = 2,3 log X
EPH = eletrodo padrão de hidrogênio
Massas Molares

Considere a seguinte configuração experimental, constituída de um canhão de partículas a,
dois detectores de partículas a posicionados ortogonalmente entre si e uma folha fina de um determinado
material (W, X, Y, Z).
Experimentos foram realizados, bombardeando cada material com uma quantidade de partículas a e registrando o número de partículas coletadas em cada detector, conforme a tabela abaixo.
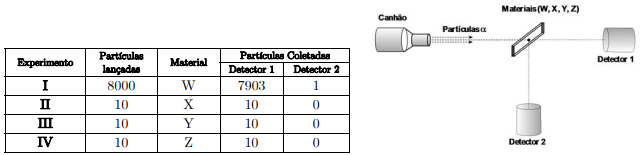
A partir dessas informações, assinale a alternativa que apresenta a conclusão CORRETA sobre as observações feitas nos experimentos.
Experimentos foram realizados, bombardeando cada material com uma quantidade de partículas a e registrando o número de partículas coletadas em cada detector, conforme a tabela abaixo.

A partir dessas informações, assinale a alternativa que apresenta a conclusão CORRETA sobre as observações feitas nos experimentos.
Q1901489
Química
Texto associado

Constantes
Constante de Avogadro (NA) = 6,02 x 1023 mol-1
Constante de Faraday (F) = 9,65 x 104 C.mol-1 = 9,65 x104 A.s.mol-1 = 9,65 x 104 J.V-1mol-1
Carga elementar = 1,60 x 10-19 C
Constante dos gases (R) = 8,21 x 10-2 atm.L.K-1.mol-1 = 8,31 J.K-1.mol-1 = 1,98 cal.K-1.mol-1
Constante de Planck (h) = 6,63 x 10-34 J.s
Velocidade da luz no vácuo = 3,0 x 108 m.s-1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 x 105 N.m-2 = 1,01325 bar
Energia: 1 J = 1 N.m = 1 kg.m2.s-2 = 6,24 x 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 ºC e 1 atm
Condições ambientes: 25 ºC e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol.L-1 (rigorosamente: atividade unitária das
espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol.L-1
ln X = 2,3 log X
EPH = eletrodo padrão de hidrogênio
Massas Molares

Sistemas compostos por água e tensoativos em diferentes proporções, depois de
homogeneizados, passam por um processo termodinâmico quando atingem temperaturas em torno de 0 °C.
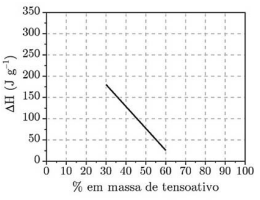
A variação de entalpia (∆H) desse processo foi determinada para cada mistura em função da composição
do sistema, conforme apresentado no gráfico. Considere que o ponto de fusão do tensoativo puro é menor
que -20 °C e o calor latente de fusão da água pura é 334 J.g-1. Sobre esses sistemas são feitas as seguintes
afirmações:
I. O ∆H refere-se à transição de fase do tensoativo.
II. O calor latente de fusão do tensoativo puro é -180 J.g-1.
III. Até 35% em massa de água pode se apresentar na forma associada à substância e não funde. IV. O ∆H é proporcional à quantidade de água não associada ao tensoativo.
Com base no gráfico e nas informações do enunciado, assinale a opção que indica a(s) afirmação(ões) CORRETA(S).
I. O ∆H refere-se à transição de fase do tensoativo.
II. O calor latente de fusão do tensoativo puro é -180 J.g-1.
III. Até 35% em massa de água pode se apresentar na forma associada à substância e não funde. IV. O ∆H é proporcional à quantidade de água não associada ao tensoativo.
Com base no gráfico e nas informações do enunciado, assinale a opção que indica a(s) afirmação(ões) CORRETA(S).

Q1901488
Química
Texto associado

Constantes
Constante de Avogadro (NA) = 6,02 x 1023 mol-1
Constante de Faraday (F) = 9,65 x 104 C.mol-1 = 9,65 x104 A.s.mol-1 = 9,65 x 104 J.V-1mol-1
Carga elementar = 1,60 x 10-19 C
Constante dos gases (R) = 8,21 x 10-2 atm.L.K-1.mol-1 = 8,31 J.K-1.mol-1 = 1,98 cal.K-1.mol-1
Constante de Planck (h) = 6,63 x 10-34 J.s
Velocidade da luz no vácuo = 3,0 x 108 m.s-1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 x 105 N.m-2 = 1,01325 bar
Energia: 1 J = 1 N.m = 1 kg.m2.s-2 = 6,24 x 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 ºC e 1 atm
Condições ambientes: 25 ºC e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol.L-1 (rigorosamente: atividade unitária das
espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol.L-1
ln X = 2,3 log X
EPH = eletrodo padrão de hidrogênio
Massas Molares

São feitas as seguintes afirmações a respeito do ciclo do oxigênio no meio ambiente:
I. A concentração de oxigênio na atmosfera está diminuindo significativamente no último século, devido à queima de combustíveis fósseis e à redução da vegetação terrestre e marinha.
II. Os maiores contribuintes para a produção de oxigênio e sua liberação na atmosfera terrestre são florestas densas, pastagens, ervas e arbustos.
III. O oxigênio está envolvido, em algum grau, em todos os outros ciclos biogeoquímicos.
IV. Águas doces frias são as maiores fontes de oxigênio livre na Terra.
Assinale a alternativa que apresentam as afirmações ERRADAS.
I. A concentração de oxigênio na atmosfera está diminuindo significativamente no último século, devido à queima de combustíveis fósseis e à redução da vegetação terrestre e marinha.
II. Os maiores contribuintes para a produção de oxigênio e sua liberação na atmosfera terrestre são florestas densas, pastagens, ervas e arbustos.
III. O oxigênio está envolvido, em algum grau, em todos os outros ciclos biogeoquímicos.
IV. Águas doces frias são as maiores fontes de oxigênio livre na Terra.
Assinale a alternativa que apresentam as afirmações ERRADAS.
Q1901486
Química
Texto associado

Constantes
Constante de Avogadro (NA) = 6,02 x 1023 mol-1
Constante de Faraday (F) = 9,65 x 104 C.mol-1 = 9,65 x104 A.s.mol-1 = 9,65 x 104 J.V-1mol-1
Carga elementar = 1,60 x 10-19 C
Constante dos gases (R) = 8,21 x 10-2 atm.L.K-1.mol-1 = 8,31 J.K-1.mol-1 = 1,98 cal.K-1.mol-1
Constante de Planck (h) = 6,63 x 10-34 J.s
Velocidade da luz no vácuo = 3,0 x 108 m.s-1
Número de Euler (e) = 2,72
Definições
Pressão: 1 atm = 760 mmHg = 1,01325 x 105 N.m-2 = 1,01325 bar
Energia: 1 J = 1 N.m = 1 kg.m2.s-2 = 6,24 x 1018 eV
Condições normais de temperatura e pressão (CNTP): 0 ºC e 1 atm
Condições ambientes: 25 ºC e 1 atm
Condições padrão: 1 bar; concentração das soluções = 1 mol.L-1 (rigorosamente: atividade unitária das
espécies); sólido com estrutura cristalina mais estável nas condições de pressão e temperatura em questão.
(s) = sólido. (ℓ) = líquido. (g) = gás. (aq) = aquoso. (conc) = concentrado. (ua) = unidades arbitrárias.
u.m.a. = unidade de massa atômica. [X] = concentração da espécie química X em mol.L-1
ln X = 2,3 log X
EPH = eletrodo padrão de hidrogênio
Massas Molares

Considere as seguintes afirmações sobre os aminoácidos:
I. Os aminoácidos são pequenas moléculas com propriedades bioquímicas únicas determinadas por seus grupos funcionais.
II. Os aminoácidos em pH fisiológico (~7,4) apresentam os grupamentos amina protonados, enquanto os grupos carboxílicos assumem sua forma de base conjugada.
III. Os aminoácidos podem se polimerizar por meio de reações de adição para formar as ligações peptídicas (CO-NH).
IV. As variações no comprimento e sequência de aminoácidos de polipeptídios são características que contribuem para a diversidade na forma e nas funções biológicas das proteínas.
V. Todos os aminoácidos obtidos de polipeptídios são opticamente ativos, isto é, eles desviam o plano da luz polarizada.
Assinale a alternativa que apresenta as afirmações CORRETAS.
I. Os aminoácidos são pequenas moléculas com propriedades bioquímicas únicas determinadas por seus grupos funcionais.
II. Os aminoácidos em pH fisiológico (~7,4) apresentam os grupamentos amina protonados, enquanto os grupos carboxílicos assumem sua forma de base conjugada.
III. Os aminoácidos podem se polimerizar por meio de reações de adição para formar as ligações peptídicas (CO-NH).
IV. As variações no comprimento e sequência de aminoácidos de polipeptídios são características que contribuem para a diversidade na forma e nas funções biológicas das proteínas.
V. Todos os aminoácidos obtidos de polipeptídios são opticamente ativos, isto é, eles desviam o plano da luz polarizada.
Assinale a alternativa que apresenta as afirmações CORRETAS.