Questões da Prova Exército - 2010 - EsFCEx - Oficial - Magistério Química
Foram encontradas 40 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Considere a equação abaixo para responder a questão.

Considere a equação abaixo para responder a questão.

I. o composto (a) é o ácido conjugado da piridina.
II. o composto (a) é base mais forte que (b) e (c).
III. os grupos metil aumentam a força básica da piridina.
IV. o composto (b) é um ácido mais fraco que (c).
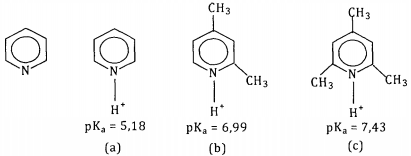
Das informações dadas estão corretas:
( ) Espécies químicas que têm na sua composição hidrogênio com carga parcial positiva, Hδ+, são ácidos de Arrhenius.
( ) Bases de Brönsted-Lowry têm na sua composição átomos com pares de elétrons não-ligantes.
( ) Bases de Brönsted-Lowry, em água, produzem íons OH-.
( ) Ácidos de Arrhenius são substâncias iônicas.
I. Segundo o princípio de Le Châtelier a adição de H+ ao sistema tampão faz liberar mesma quantidade de OH-.
II. O sistema tampão funciona no sistema digestivo, mas não no sistema sanguíneo.
III. Por adição do sal à solução do ácido para formar o tampão, a percentagem de dissociação do ácido diminui.
IV. A solução tampão sofre pequena variação de pH quando a ela são adicionados íons H+ ou OH-.