Neste ano de 2019, foi realizada pelos alunos da EsPCE...
Neste ano de 2019, foi realizada pelos alunos da EsPCEx uma prática no laboratório de química envolvendo eletrólise com eletrodos ativos conforme a descrição experimental:
- Num béquer de capacidade 100 mL (cuba eletrolítica) coloque cerca de 50 mL de solução aquosa de sulfato de cobre II de concentração 1 mol.L-1. Tome como eletrodos uma barra fina de cobre e um prego de ferro. Ligue-os com auxílio de fios a uma fonte externa de eletricidade com uma corrente contínua de intensidade de 3 Ampères. Esta fonte tem capacidade para efetuar perfeitamente esse processo de eletrólise. O prego deve ser ligado ao polo negativo da fonte e a barra de cobre ao polo positivo da fonte. Mergulhe os eletrodos na solução durante 16 minutos e 5 segundos e observe.
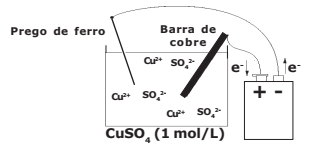
Considere o arranjo eletrolítico (a 25 ºC e 1 atm) e o sal completamente dissociado, conforme visto na figura a seguir:
Dado: 1 Faraday (F) = 96500 Coulomb (C) / mol de elétrons
Na discussão apresentada nos relatórios dos diversos grupos de alunos, surgiram as seguintes afirmativas:
I – Na superfície do prego ocorreu a deposição de cobre metálico.
II – Durante o processo a barra de cobre se oxida.
III – A massa de cobre metálico que se depositou na superfície do prego foi de 2,45 g.
IV – A semi-reação de redução que ocorre no cátodo é Cu2+ + 2 e- → Cuº.
V – A reação global é Fe2+ + Cuº → Feº + Cu2+