Questões de Concurso Militar PM-PR 2018 para Aspirante da Polícia Militar
Foram encontradas 9 questões
A fórmula mínima desse óxido é:
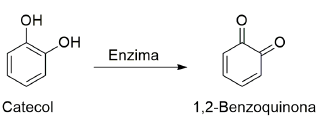
A respeito do fenômeno descrito acima, considere as seguintes afirmativas:
1. Na estrutura do catecol está presente a função orgânica fenol. 2. O catecol e a 1,2-benzoquinona são isômeros espaciais (enantiômeros). 3. A transformação do catecol em 1,2-benzoquinona é uma reação de oxidação. 4. Todos os átomos de carbono na estrutura da 1,2-benzoquinona possuem hibridização sp3 .
Assinale a alternativa correta.
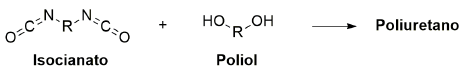
A estrutura química da unidade de repetição desse polímero é:
Constantes de equilíbrio de ácidos fracos a 25 oC

Com base nas informações fornecidas, qual dos sais indicados a seguir é o mais eficiente como solução neutralizante?