Questões de Concurso Militar EsPCEx 2008 para Cadete do Exército - 1° Dia
Foram encontradas 11 questões
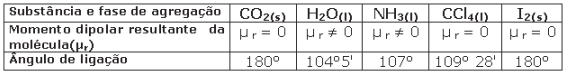
A alternativa que relaciona corretamente a molécula da substância, a polaridade dessa molécula, a forma geométrica dessa molécula e o tipo de força intermolecular dessa substância, nessa ordem, é:
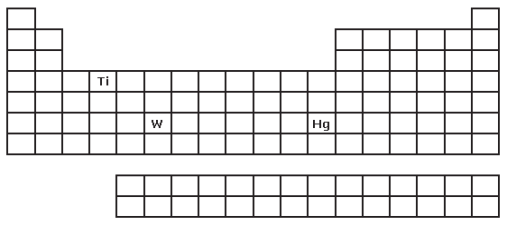
I) É freqüentemente usado em lâmpadas incandescentes, tem elevado ponto de fusão e número atômico igual 74.
II) É líquido nas condições ambiente (25º C e 1 atm) e utilizado em barômetros, em lâmpadas especiais e em odontologia.
III) Possui número atômico 22 e está na família 4 da Tabela Periódica. Algumas de suas utilizações podem ser assim exemplificadas: aplicação de próteses em joelhos e quadris; colocação de pinos para fixação entre a mandíbula e a prótese dentária.
Os metais descritos em I, II e III são, respectivamente:
O luminol (C8H7O3N3) é um reagente de quimioluminiscência utilizado pela polícia para detectar vestígios de sangue.
Em relação aos elementos químicos C, H, O e N que compõem o luminol, pode-se afirmar
que:

Cl2(g) + OH1-(aq) → Cl1-(aq) + ClO31-(aq) + H2O(l)
Bicarbonato 100,0
Cálcio 22,0
Sódio 8,98
Nitrato 4,11
Sulfato 6,00
Magnésio 3,26
Potássio 2,70
Cloreto 0,73
Fluoreto 0,34
Sabe-se que a massa molar do íon sulfato (SO42-) é de 96 g/mol. A quantidade de mols de íons sulfato contida em 16 L dessa água mineral é: