Questões Militares de Química - Transformações Químicas: elementos químicos, tabela periódica e reações químicas
Foram encontradas 111 questões
Em condições ideais, pequenas quantidades de gás cloro podem ser geradas em laboratório pela reação do óxido de manganês (MnO2 ) com ácido clorídrico (HCl), conforme a equação química a seguir não balanceada.
HCl(aq) + MnO2 (s) → H2O(L) + MnCl2(s) + Cl2(g)
A partir dessas informações, quantas moléculas de gás cloro, aproximadamente, podem ser produzidas quando 10 g de óxido de manganês com grau de pureza de 87% são colocados para reagir completamente com excesso de ácido clorídrico?
Dado: Número de Avogadro (N) = 6 x 1023
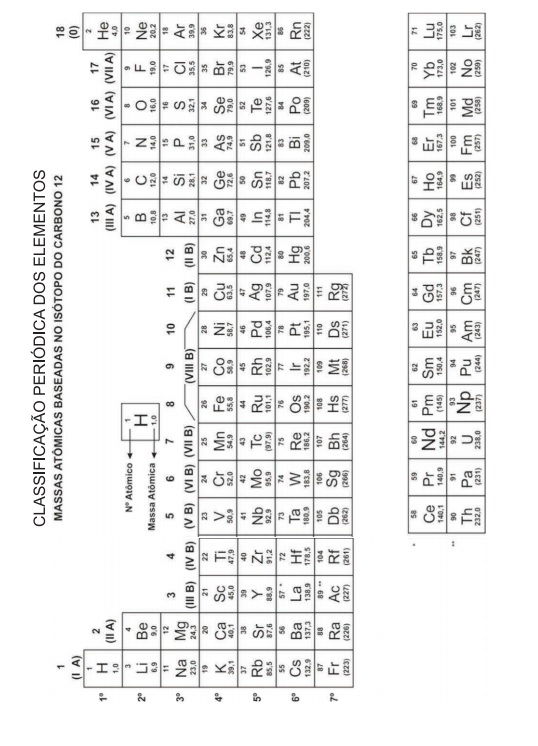
A tabela periódica é uma das realizações mais notáveis da Química porque ajuda a organizar a extensa quantidade de propriedades dos elementos, que, de outra forma, seria um arranjo confuso. A tabela periódica pode ser usada na previsão de um grande número de propriedades, muitas das quais são cruciais para a compreensão das características químicas e físicas dos compostos.
Sobre as propriedades periódicas dos átomos, pode-se afirmar que
Com relação à química, coloque verdadeiro (V) ou (F) nas afirmativas abaixo, a seguir, a opção correta.
( ) Compostos moleculares são formados por meio de ligações metálicas.
( ) Uma substância formada pela ligação entre um metal e um ametal é iônica.
( ) Na tabela periódica, elementos presentes na coluna 17 tendem a receber elétrons, enquanto que os presentes na coluna 1 tendem a doar elétrons.
( ) A tabela periódica atual foi organizada baseada no número atômico dos elementos.
( ) Os gases nobres são elementos que reagem facilmente com qualquer outro elemento.
( ) Um elemento X- e um elemento Y2+ formarão um composto iônico X2Y.
A pólvora é material empregado como propulsor em armas de fogo. Basicamente, a ideia é provocar uma reação que gere uma quantidade grande de gases sob pressão e temperatura elevadas. Ao se expandirem, esses gases impulsionam um projétil. A pólvora negra, empregada em armas mais antigas, é constituída por uma mistura de salitre (KNO3), enxofre (S) e material de carbono (C). A equação não balanceada de uma das reações químicas que ocorrem durante a queima da pólvora é apresentada a seguir.
KNO3 (s) + S (s) + C (s) → K2S (s) + N2 (g) + CO2 (g)
Considerando essas informações e sabendo que o número atômico do carbono é igual a 6, julgue o item que se segue.
Entre os produtos da reação química apresentada, podem ser
identificadas uma substância iônica e duas substâncias
moleculares; entre as substâncias moleculares, uma é polar e,
a outra, apolar.
Com relação a reações químicas e a substâncias, julgue o item subsequente.
Um átomo de carbono pode formar 2, 4 ou 6 ligações com
outro átomo de carbono.