Questões Militares de Engenharia Química e Química Industrial - Termodinâmica e Equilíbrio de Fases
Foram encontradas 98 questões
Uma central termoelétrica, capaz de gerar 50 MW de potência, opera a uma eficiência térmica máxima de 40%.
A taxa de energia dissipada para o ambiente é
Na figura a seguir, é apresentado o diagrama de equilíbrio para sistema SO2(g) – H2O(l), no qual é expressa a solubilidade do dióxido de enxofre na água como uma função da pressão do gás e da temperatura do sistema.
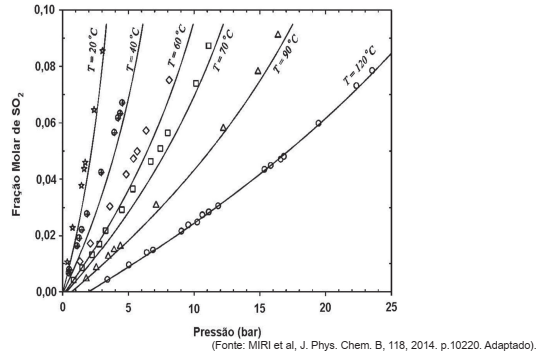
Com base nessa figura, avalie o que se afirma.
I. O aumento da pressão exercida pelo gás favorece a absorção do SO2 (g) pela água.
II. O aumento da temperatura aumenta a capacidade de absorção do SO2 (g) pelo solvente.
III. Na temperatura T = 20° , a absorção ocorre mais rapidamente que à temperatura T = 120° .
Está correto apenas o que se afirma em
Deseja-se fundir 115 g de sódio metálico, inicialmente a 291 K e 1 bar, sendo a energia de transição de fase, à temperatura de transição e 1 bar, igual a 2,6 kJ.mol-1, conforme indicado a seguir.

Sabendo-se que a massa molar do sódio metálico é igual a 23,0 g.mol-1 e considerando-se a capacidade
calorífica molar do sódio metálico constante no intervalo de temperatura utilizado e igual a 28,0 J.K-1.mol-1, é
correto afirmar que a energia necessária para realizar a fusão, a 1 bar e 371k , é
Na figura a seguir, é apresentado o diagrama de equilíbrio de fases sólido-líquido, em função da temperatura, à pressão constante, para o sistema CaCl2 -H2O.
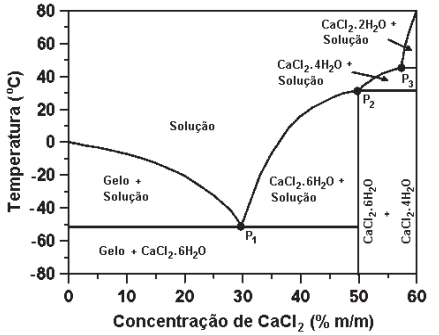
(Disponível em:<https://engineering.purdue.edu/JTRP/Highlights/cacl2-dihydrate-cacl2-2h2o> . Acesso em: 9 fev. 2019. Adaptado.)
Observe o que se afirma a partir desse diagrama.
I. Os pontos P1, P2 e P3 correspondem às diferentes composições eutéticas do sistema.
II. O ponto P1 é o único que corresponde à mistura eutética e há três fases em equilíbrio neste ponto.
III. Independentemente da composição da mistura, à temperatura de 60° C, há somente uma fase presente.
IV. Para qualquer composição da mistura ou condição de temperatura, não é possível obter as fases H2O(s) e CaCl2 .4H2O(s) em equilíbrio.
Uma das ferramentas que pode auxiliar nos estudos de obtenção de tampões ou até mesmo de precipitação, é o digrama de especiação. Nesse diagrama, podem ser observadas as espécies presentes no meio para diferentes valores de pH e suas concentrações (representadas como pC, que é o negativo do logaritmo das concentrações). A seguir, está apresentado o diagrama de especiação do ácido cianídrico, a 25°C para uma concentração total de cianeto igual a 10-3mol/L (pC=3). O ácido cianídrico é altamente tóxico, no entanto é largamente utilizado no tratamento de ouro.
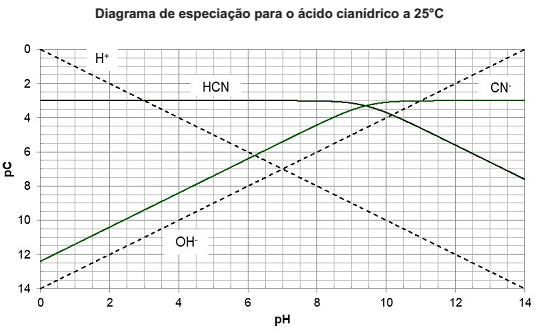
A partir do diagrama, considerando que uma solução com concentração de 10-3mol/L de ácido cianídrico seja
ideal, a 25°C, em um recipiente fechado, o pH da solução será igual a