Questões do Enem
Foram encontradas 132 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
O ferro é encontrado na natureza na forma de seus minérios, tais como a hematita (α-Fe2 O3), a magnetita (Fe3O4) e a wustita (FeO). Na siderurgia, o ferro-gusa é obtido pela fusão de minérios de ferro em altos fornos em condições adequadas. Uma das etapas nesse processo é a formação de monóxido de carbono. O CO (gasoso) é utilizado para reduzir o FeO (sólido), conforme a equação química:
FeO (s) + CO (g) → Fe (s) + CO2(g)
Considere as seguintes equações termoquímicas:
Fe2O3 (s) + 3 CO (g) → 2 Fe (s) + 3 CO2 (g) ΔrH = -25 kJ/mol de Fe2O3
= -25 kJ/mol de Fe2O3
3 FeO (s) + CO2 (g) → Fe3O4 (s) + CO (g) ΔrH = -36 kJ/mol de CO2
= -36 kJ/mol de CO2
2 Fe3O4 (s) + CO2 (g) → 3 Fe2O3 (s) + CO (g) ΔrH = +47 kJ/mol de CO2
= +47 kJ/mol de CO2
O valor mais próximo de ΔrH , em kJ/mol de FeO, para a reação indicada do FeO (sólido) com o CO (gasoso) é
, em kJ/mol de FeO, para a reação indicada do FeO (sólido) com o CO (gasoso) é
A invenção do LED azul, que permite a geração de outras cores para compor a luz branca, permitiu a construção de lâmpadas energeticamente mais eficientes e mais duráveis do que as incandescentes e fluorescentes. Em um experimento de laboratório, pretende-se associar duas pilhas em série para acender um LED azul que requer 3,6 volts para o seu funcionamento. Considere as semirreações de redução e seus respectivos potenciais mostrados no quadro.

Qual associação em série de pilhas fornece diferença de potencial, nas condições-padrão, suficiente para acender o LED azul?
As centrífugas são equipamentos utilizados em laboratórios, clínicas e indústrias. Seu funcionamento faz uso da aceleração centrífuga obtida pela rotação de um recipiente e que serve para a separação de sólidos em suspensão em líquidos ou de líquidos misturados entre si.
RODITI, I. Dicionário Houaiss de física. Rio de Janeiro: Objetiva, 2005 (adaptado).
Nesse aparelho, a separação das substâncias ocorre em função
A farinha de linhaça dourada é um produto natural que oferece grandes benefícios para o nosso organismo. A maior parte dos nutrientes da linhaça encontra-se no óleo desta semente, rico em substâncias lipossolúveis com massas moleculares elevadas. A farinha também apresenta altos teores de fibras proteicas insolúveis em água, celulose, vitaminas lipossolúveis e sais minerais hidrossolúveis.
Considere o esquema, que resume um processo de separação dos componentes principais da farinha de linhaça dourada.
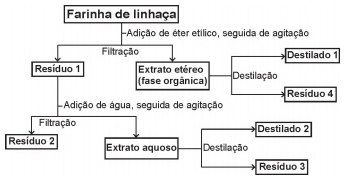
O óleo de linhaça será obtido na fração
Na Idade Média, para elaborar preparados a partir de plantas produtoras de óleos essenciais, as coletas das espécies eram realizadas ao raiar do dia. Naquela época, essa prática era fundamentada misticamente pelo efeito mágico dos raios lunares, que seria anulado pela emissão dos raios solares. Com a evolução da ciência, foi comprovado que a coleta de algumas espécies ao raiar do dia garante a obtenção de material com maiores quantidades de óleos essenciais.
A explicação científica que justifica essa prática se baseia na
A técnica do carbono-14 permite a datação de fósseis pela medição dos valores de emissão beta desse isótopo presente no fóssil. Para um ser em vida, o máximo são 15 emissões beta/(min g). Após a morte, a quantidade de 14C se reduz pela metade a cada 5 730 anos.
A prova do carbono 14. Disponível em: http://noticias.terra.com.br. Acesso em: 9 nov. 2013 (adaptado).
Considere que um fragmento fóssil de massa igual a 30 g foi encontrado em um sítio arqueológico, e a medição de radiação apresentou 6 750 emissões beta por hora. A idade desse fóssil, em anos, é
Partículas microscópicas existentes na atmosfera funcionam como núcleos de condensação de vapor de água que, sob condições adequadas de temperatura e pressão, propiciam a formação das nuvens e consequentemente das chuvas. No ar atmosférico, tais partículas são formadas pela reação de ácidos (HX com a base NH3, de forma natural ou antropogênica, dando origem a sais de amônio (NH4X , de acordo com a equação química genérica:
HX (g) + NH3 (g) → NH4X (s)
FELIX, E. P.; CARDOSO, A. A. Fatores ambientais que afetam a precipitação úmida. Química Nova na Escola, n. 21, maio 2005 (adaptado).
A fixação de moléculas de vapor de água pelos núcleos
de condensação ocorre por
A eletrólise é um processo não espontâneo de grande importância para a indústria química. Uma de suas aplicações é a obtenção do gás cloro e do hidróxido de sódio, a partir de uma solução aquosa de cloreto de sódio. Nesse procedimento, utiliza-se uma célula eletroquímica, como ilustrado.
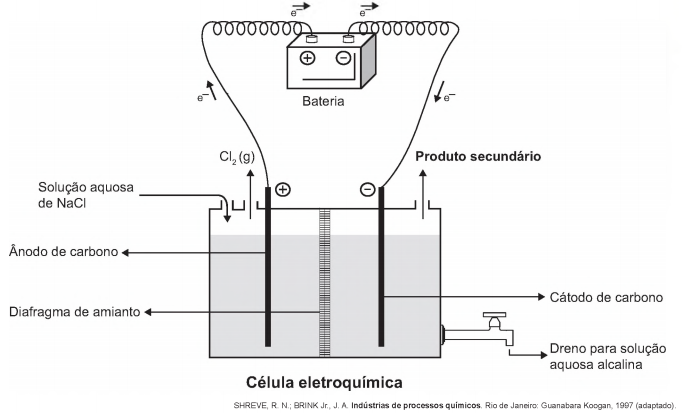
No processo eletrolítico ilustrado, o produto secundário obtido é o
A obtenção de energia por meio da fissão nuclear do 235U é muito superior quando comparada à combustão da gasolina. O calor liberado na fissão do 235U é 8 x 1010 J/g e na combustão da gasolina é 5 x 104 J/g.
A massa de gasolina necessária para obter a mesma energia na fissão de 1 kg de 235U é da ordem de
Para comparar a eficiência de diferentes combustíveis, costuma-se determinar a quantidade de calor liberada na combustão por mol ou grama de combustível. O quadro mostra o valor de energia liberada na combustão completa de alguns combustíveis.
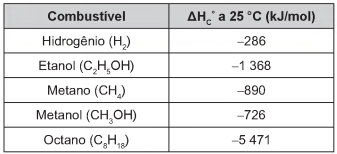
As massas molares dos elementos H, C e O são iguais a 1 g/mol, 12 g/mol e 16 g/mol, respectivamente.
ATKINS, P Princípios de química. Porto Alegre: Bookman, 2007 (adaptado).
Qual combustível apresenta maior liberação de energia
por grama?
Atualmente, soldados em campo, seja em treinamento ou em combate, podem aquecer suas refeições, prontas e embaladas em bolsas plásticas, utilizando aquecedores químicos, sem precisar fazer fogo. Dentro dessas bolsas existe magnésio metálico em pó e, quando o soldado quer aquecer a comida, ele coloca água dentro da bolsa, promovendo a reação descrita pela equação química:
Mg (s) + 2 H2O (I) → Mg(OH)2 (s) + H2 (g) + 350 kJ
O aquecimento dentro da bolsa ocorre por causa da
A crescente produção industrial lança ao ar diversas substâncias tóxicas que podem ser removidas pela passagem do ar contaminado em tanques para filtração por materiais porosos, ou para dissolução em água ou solventes orgânicos de baixa polaridade, ou para neutralização em soluções ácidas ou básicas. Um dos poluentes mais tóxicos liberados na atmosfera pela atividade industrial é a 2,3,7,8-tetraclorodioxina.
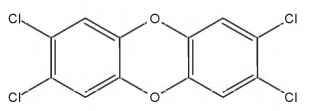
Esse poluente pode ser removido do ar pela passagem através de tanques contendo
O quadro apresenta alguns exemplos de combustíveis empregados em residências, indústrias e meios de transporte.
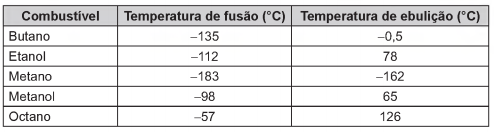
São combustíveis líquidos à temperatura ambiente de 25 ºC:
A energia nuclear é uma alternativa aos combustíveis fósseis que, se não gerenciada de forma correta, pode causar impactos ambientais graves. O princípio da geração dessa energia pode se basear na reação de fissão controlada do urânio por bombardeio de nêutrons, como ilustrado:
235U + n → 95Sr + 139Xe + 2 n + energia
Um grande risco decorre da geração do chamado lixo atômico, que exige condições muito rígidas de tratamento e armazenamento para evitar vazamentos para o meio ambiente.
Esse lixo é prejudicial, pois
O ambiente marinho pode ser contaminado com rejeitos radioativos provenientes de testes com armas nucleares. Os materiais radioativos podem se acumular nos organismos. Por exemplo, o estrôncio-90 é quimicamente semelhante ao cálcio e pode substituir esse elemento nos processos biológicos.
FIGUEIRA, R. C. L.; CUNHA, I. I. L. A contaminação dos oceanos por radionuclídeos antropogênicos. Química Nova na Escola, n. 1, 1998 (adaptado).
Um pesquisador analisou as seguintes amostras coletadas em uma região marinha próxima a um local que manipula o estrôncio radioativo: coluna vertebral de tartarugas, concha de moluscos, endoesqueleto de ouriços-do-mar, sedimento de recife de corais e tentáculos de polvo.
Em qual das amostras analisadas a radioatividade foi
menor?
A obtenção do alumínio dá-se a partir da bauxita (Al2O3 .3H2O), que é purificada e eletrolisada numa temperatura de 1 000 °C. Na célula eletrolítica, o ânodo é formado por barras de grafita ou carvão, que são consumidas no processo de eletrólise, com formação de gás carbônico, e o cátodo é uma caixa de aço coberta de grafita.
A etapa de obtenção do alumínio ocorre no
Em Bangladesh, mais da metade dos poços artesianos cuja água serve à população local está contaminada com arsênio proveniente de minerais naturais e de pesticidas. O arsênio apresenta efeitos tóxicos cumulativos. A ONU desenvolveu um kit para tratamento dessa água a fim de torná-la segura para o consumo humano. O princípio desse kit é a remoção do arsênio por meio de uma reação de precipitação com sais de ferro(III) que origina um sólido volumoso de textura gelatinosa.
Disponível em: http://tc.iaea.org. Acesso em: 11 dez. 2012 (adaptado).
Com o uso desse kit, a população local pode remover o elemento tóxico por meio de
Utensílios de uso cotidiano e ferramentas que contêm ferro em sua liga metálica tendem a sofrer processo corrosivo e enferrujar. A corrosão é um processo eletroquímico e, no caso do ferro, ocorre a precipitação do óxido de ferro(III) hidratado, substância marrom pouco solúvel, conhecida como ferrugem. Esse processo corrosivo é, de maneira geral, representado pela equação química:
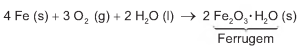
Uma forma de impedir o processo corrosivo nesses
utensílios é
Uma pessoa é responsável pela manutenção de uma sauna úmida. Todos os dias cumpre o mesmo ritual: colhe folhas de capim-cidreira e algumas folhas de eucalipto. Em seguida, coloca as folhas na saída do vapor da sauna, aromatizando-a, conforme representado na figura.
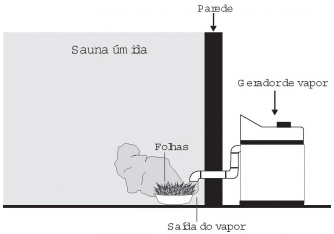
Qual processo de separação é responsável pela
aromatização promovida?
Primeiro, em relação àquilo a que chamamos água, quando congela, parece-nos estar a olhar para algo que se tornou pedra ou terra, mas quando derrete e se dispersa, esta torna-se bafo e ar; o ar, quando é queimado, torna-se fogo; e, inversamente, o fogo, quando se contrai e se extingue, regressa à forma do ar; o ar, novamente concentrado e contraído, torna-se nuvem e nevoeiro, mas, a partir destes estados, se for ainda mais comprimido, torna-se água corrente, e de água torna-se novamente terra e pedras; e deste modo, como nos parece, dão geração uns aos outros de forma cíclica.
PLATÃO. Timeu-Crítias. Coimbra: CECH, 2011.
Do ponto de vista da ciência moderna, os “quatro elementos” descritos por Platão correspondem, na verdade, às fases sólida, líquida, gasosa e plasma da matéria. As transições entre elas são hoje entendidas como consequências macroscópicas de transformações sofridas pela matéria em escala microscópica.