Questões do Enem
Foram encontradas 136 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2023
Banca:
INEP
Órgão:
ENEM
Prova:
INEP - 2023 - ENEM - Exame Nacional do Ensino Médio - Primeiro e Segundo Dia - Edital 2023 |
Q2336274
Química
O descarte de detergentes comuns nos esgotos
domésticos ocasiona a formação de uma camada
de espuma que impede a entrada de oxigênio na
água. Os microrganismos que vivem nessas águas
não são capazes de quebrar moléculas ramificadas,
ocorrendo assim um desequilíbrio ambiental nos rios.
A fórmula a seguir representa a estrutura química de um
tensoativo presente na composição de um detergente
não biodegradável.
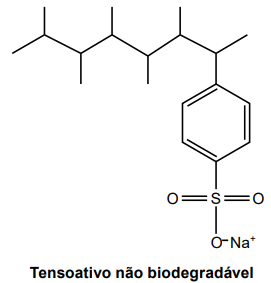
Qual modificação química na estrutura desse tensoativo o tornaria um detergente biodegradável?

Qual modificação química na estrutura desse tensoativo o tornaria um detergente biodegradável?
Ano: 2023
Banca:
INEP
Órgão:
ENEM
Prova:
INEP - 2023 - ENEM - Exame Nacional do Ensino Médio - Primeiro e Segundo Dia - Edital 2023 |
Q2336272
Química
O consumo exagerado de refrigerantes é preocupante,
pois contribui para o aumento de casos de obesidade e
diabetes. Considere dois refrigerantes enlatados, um
comum e um diet, e que ambos possuam a mesma
quantidade de aditivos, exceto pela presença de
açúcar. O refrigerante comum contém basicamente
água carbonatada e grande quantidade de açúcar;
já o refrigerante diet tem água carbonatada e adoçantes,
cujas massas são muito pequenas.
CAVAGIS, A. D. M.; PEREIRA, E. A.; OLIVEIRA, L. C. Um método simples para avaliar o teor de sacarose e CO2 em refrigerantes. Química Nova na Escola, n. 3, ago. 2014 (adaptado).
Entre as duas versões apresentadas, o refrigerante comum possui
CAVAGIS, A. D. M.; PEREIRA, E. A.; OLIVEIRA, L. C. Um método simples para avaliar o teor de sacarose e CO2 em refrigerantes. Química Nova na Escola, n. 3, ago. 2014 (adaptado).
Entre as duas versões apresentadas, o refrigerante comum possui
Ano: 2023
Banca:
INEP
Órgão:
ENEM
Prova:
INEP - 2023 - ENEM - Exame Nacional do Ensino Médio - Primeiro e Segundo Dia - Edital 2023 |
Q2336271
Química
Uma cafeteria adotou copos fabricados a partir
de uma composição de 50% de plástico reciclado não
biodegradável e 50% de casca de café. O copo é reutilizável
e retornável, pois o material, semelhante a uma cerâmica,
suporta a lavagem. Embora ele seja comercializado por
um preço considerado alto quando comparado ao de um
copo de plástico descartável, essa cafeteria possibilita aos
clientes retornarem o copo sujo e levarem o café quente
servido em outro copo já limpo e higienizado. O material
desse copo oferece também o conforto de não esquentar
na parte externa.
Cafeteria adota copo reutilizável feito com casca de café. Disponível em: www.gazetadopovo.com.br. Acesso em: 5 dez. 2019 (adaptado).
Quais duas vantagens esse copo apresenta em comparação ao copo descartável?
Cafeteria adota copo reutilizável feito com casca de café. Disponível em: www.gazetadopovo.com.br. Acesso em: 5 dez. 2019 (adaptado).
Quais duas vantagens esse copo apresenta em comparação ao copo descartável?
Ano: 2023
Banca:
INEP
Órgão:
ENEM
Prova:
INEP - 2023 - ENEM - Exame Nacional do Ensino Médio - Primeiro e Segundo Dia - Edital 2023 |
Q2336263
Química
Em uma indústria alimentícia, para produção de doce de leite, utiliza-se um tacho de parede oca com uma entrada
para vapor de água a 120 °C e uma saída para água líquida em equilíbrio com o vapor a 100 °C. Ao passar pela parte
oca do tacho, o vapor de água transforma-se em líquido, liberando energia. A parede transfere essa energia para o
interior do tacho, resultando na evaporação de água e consequente concentração do produto.
No processo de concentração do produto, é utilizada energia proveniente
No processo de concentração do produto, é utilizada energia proveniente
Ano: 2023
Banca:
INEP
Órgão:
ENEM
Prova:
INEP - 2023 - ENEM - Exame Nacional do Ensino Médio - Primeiro e Segundo Dia - Edital 2023 |
Q2336251
Química
Um assistente de laboratório precisou descartar sete frascos contendo solução de nitrato de mercúrio(I) que não
foram utilizados em uma aula prática. Cada frasco continha 5,25 g de Hg2
(NO3
)2
dissolvidos em água. Temendo a
toxidez do mercúrio e sabendo que o Hg2Cl2
tem solubilidade muito baixa, o assistente optou por retirar o mercúrio da
solução por precipitação com cloreto de sódio (NaCl), conforme a equação química:
Hg2(NO3 )2 (aq) + 2 NaCl (aq) ➝ Hg2Cl2 (s) + 2 NaNO3 (aq)
Na dúvida sobre a massa de NaCl a ser utilizada, o assistente aumentou gradativamente a quantidade adicionada em cada frasco, como apresentado no quadro.
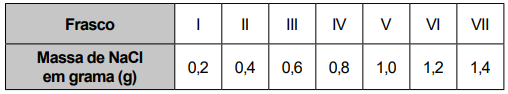
O produto obtido em cada experimento foi filtrado, secado e teve sua massa aferida. O assistente organizou os resultados na forma de um gráfico que correlaciona a massa de NaCl adicionada com a massa de Hg2Cl2 obtida em cada frasco. A massa molar do Hg2 (NO3 )2 é 525 g mol–1, a do NaCl é 58 g mol–1 e a do Hg2Cl2 é 472 g mol–1.
Qual foi o gráfico obtido pelo assistente de laboratório?
Hg2(NO3 )2 (aq) + 2 NaCl (aq) ➝ Hg2Cl2 (s) + 2 NaNO3 (aq)
Na dúvida sobre a massa de NaCl a ser utilizada, o assistente aumentou gradativamente a quantidade adicionada em cada frasco, como apresentado no quadro.

O produto obtido em cada experimento foi filtrado, secado e teve sua massa aferida. O assistente organizou os resultados na forma de um gráfico que correlaciona a massa de NaCl adicionada com a massa de Hg2Cl2 obtida em cada frasco. A massa molar do Hg2 (NO3 )2 é 525 g mol–1, a do NaCl é 58 g mol–1 e a do Hg2Cl2 é 472 g mol–1.
Qual foi o gráfico obtido pelo assistente de laboratório?