Questões de Vestibular UFCG 2009 para Vestibular - Segunda Etapa - Dia 2
Foram encontradas 40 questões
Q1370178
Química
Na fabricação de cerveja, adiciona-se gás carbônico durante o processo de engarrafamento (parte do CO2 já é produzida
durante a fermentação). Isso faz com que o produto final apresente uma acidez maior devido à hidrólise de CO2 ,que produz o ácido
carbônico, H2CO3. Por outro lado, o CO2 em solução fica em equilíbrio com o CO2 não solubilizado, como representado a seguir:
CO2(g) ↔ CO2(aq) ΔH = –14,8 kJ/mol
Suponha que a geração de espuma esteja relacionada à quantidade de gás liberado durante a abertura da garrafa e que duas garrafas sejam abertas no mesmo bar, uma a 6 oC e outra a 25 oC.
Em relação à acidez da cerveja, pode-se concluir que:
CO2(g) ↔ CO2(aq) ΔH = –14,8 kJ/mol
Suponha que a geração de espuma esteja relacionada à quantidade de gás liberado durante a abertura da garrafa e que duas garrafas sejam abertas no mesmo bar, uma a 6 oC e outra a 25 oC.
Em relação à acidez da cerveja, pode-se concluir que:
Q1370179
Química
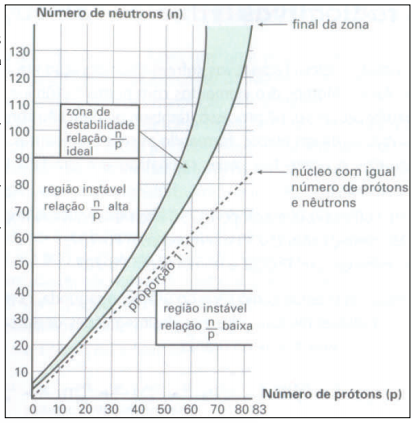
Dentre os 330 isótopos naturais, cerca de 270 são estáveis, os outros se desintegram espontaneamente. É a radioatividade natural. A relação (A – Z) / Z permite determinar se o isótopo de um elemento apresentará radioatividade natural. Isto ocorre quando esta relação é superior ou igual a 1,5. A figura abaixo relaciona o número de prótons e o número de nêutrons para os núcleos dos átomos dos elementos que, em função da relação n/p, permitem prever o tipo de desintegração sofrido por este elemento, caso este elemento apresentar radioatividade natural. A partir da análise da figura e considerando 5 isótopos hipotéticos chamados E1, E2, E3, E4 e E5, seria possível afirmar que:
Q1370180
Química
Um composto cíclico é completamente livre de tensão
quando o calor de formação obtido experimentalmente é igual
ao calor de formação do ciclo sem tensão. Admitindo que o
ciclohexano seja completamente livre de tensão, e como a
fórmula geral dos cicloalcanos pode ser representada por
(CH2)n , a quantidade de energia com que cada grupo CH2
contribuiria para a formação do ciclo sem tensão, é de –20,6
kJ. Assim, é possível calcular para cada cicloalcano a energia
correspondente à tensão do ciclo e prever a estabilidade
deste composto. A tensão do ciclo será a diferença entre o
calor de formação sem tensão e o calor de formação
experimental.
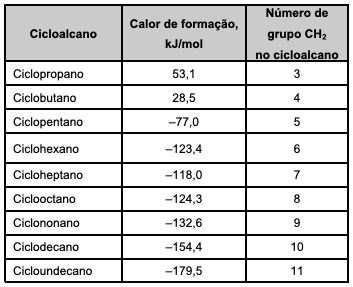
Utilizando a tabela, pode-se afirmar que:

Utilizando a tabela, pode-se afirmar que:
Q1370181
Química
Cinco gases, G1, G2, G3, G4 e G5, encontram-se
armazenados em cinco cilindros diferentes sem se saber qual
gás está em qual cilindro. Vários experimentos foram
realizados para tentar identificá-los.
Dos 5 gases, 2 são considerados combustíveis (G1 e
G2). Mas, ao passar os produtos da combustão destes gases
por um tubo contendo cloreto de cálcio anidro (usado para
absorver água), houve aumento de massa desse tubo apenas
no caso do gás G1.
Ao preparar uma solução aquosa por borbulhamento
dos gases em água, somente a solução do gás G3 fez a
fenolftaleína mudar de cor, passando de incolor à violeta.
Apenas G4 e G5 produziram precipitado quando
borbulhados em água de cal. G4 e G5 foram então
borbulhados em uma solução aquosa ácida de permanganato
de potássio, de coloração violeta. Apenas o gás G4 sofreu
oxidação, portanto descorou a solução.
Assinale a sequência que identifica corretamente os cinco gases:
Assinale a sequência que identifica corretamente os cinco gases:
Q1370182
Química
O. Diels e K. Alder foram contemplados com o prêmio Nobel em 1950, pela descoberta de uma reação química importante,
que consiste na formação de um composto cíclico, a partir de um composto com duplas ligações alternadas entre átomos de
carbono e outro composto, com pelo menos uma dupla ligação, entre átomos de carbono, chamado de dienófilo, como
exemplificado abaixo:
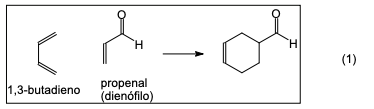
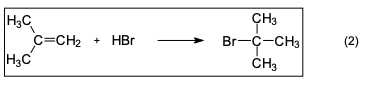
Compostos com duplas ligações entre átomos de carbono podem reagir com HBr, sob condições adequadas, como indicado:
Considerando os compostos I, II e III, cuja estrutura molecular é mostrada abaixo,
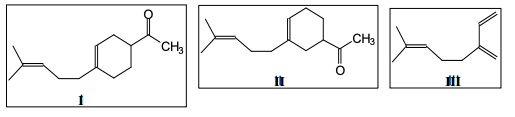
e considerando que os compostos que reagem com III para formar I e II são os dienófilos IV e V, respectivamente, escolha a alternativa correta.

Compostos com duplas ligações entre átomos de carbono podem reagir com HBr, sob condições adequadas, como indicado:

Considerando os compostos I, II e III, cuja estrutura molecular é mostrada abaixo,

e considerando que os compostos que reagem com III para formar I e II são os dienófilos IV e V, respectivamente, escolha a alternativa correta.