Questões de Vestibular UEFS 2010 para Vestibular, Prova 03
Foram encontradas 60 questões
A evolução, assim como a replicação do ácido nucleico, própria da reprodução e da autopoese — capacidade de auto-organização e autorregeneração dos seres vivos —, é um “tropeço para adiante”, destinado a protelar a ameaça da dissolução termodinâmica. A maioria dos átomos de nossos corpos é feita de hidrogênio — o elemento que, como gás, de acordo com os modelos astronômicos, foi explosivamente deslocado para além dos confins do sistema solar interno, quando o Sol se acendeu. Hoje em dia, gases ricos em hidrogênio, como a amônia, existem não apenas nas atmosferas dos gigantescos planetas externos, mas também no sistema solar interno, onde a vida os preservou com sua mesmíssima estrutura, desde que começou a se manter e a se reproduzir.
(MARGULIS & SAGAN, 2002, p. 92)
A evolução, assim como a replicação do ácido nucleico, própria da reprodução e da autopoese — capacidade de auto-organização e autorregeneração dos seres vivos —, é um “tropeço para adiante”, destinado a protelar a ameaça da dissolução termodinâmica. A maioria dos átomos de nossos corpos é feita de hidrogênio — o elemento que, como gás, de acordo com os modelos astronômicos, foi explosivamente deslocado para além dos confins do sistema solar interno, quando o Sol se acendeu. Hoje em dia, gases ricos em hidrogênio, como a amônia, existem não apenas nas atmosferas dos gigantescos planetas externos, mas também no sistema solar interno, onde a vida os preservou com sua mesmíssima estrutura, desde que começou a se manter e a se reproduzir.
(MARGULIS & SAGAN, 2002, p. 92)
Ao considerar as condições necessárias para se reconhecer cientificamente a possibilidade de vida em outro planeta e com base no padrão terrestre, é possível afirmar:
Conforme proposto por Alexander Oparin, na sua hipótese heterotrófica de origem da vida, esta pode ter surgido a partir de uma longa evolução química.
Com relação aos pressupostos desenvolvidos por essa hipótese e dos novos conhecimentos associados a esse tema, é possível afirmar:
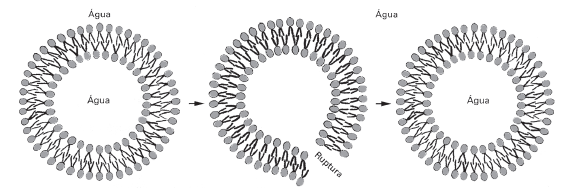
A figura ilustra o mecanismo de autosselagem presente na membrana plasmática dos seres vivos, responsável pela capacidade de autorregeneração existente nessa estrutura.
Considerando-se a importância desse fenômeno, pode-se apontar um tipo de transporte entre o meio externo e a célula que
é diretamente dependente desse mecanismo, como
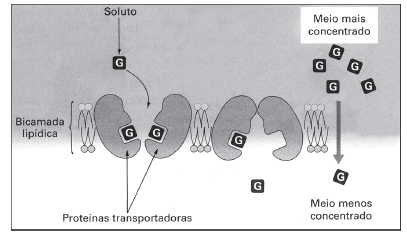
A figura ilustra o transporte de um determinado tipo de soluto através da membrana plasmática em um ambiente celular.
Em relação às características associadas a esse tipo de transporte, é correto afirmar que
A partir do entendimento das interações existentes entre o genótipo e o ambiente na expressão das informações genéticas, é correto afirmar:
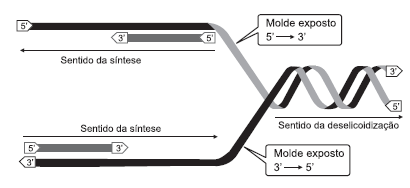
A figura ilustra um momento do processo de duplicação do material genético presente nos seres vivos.
É possível afirmar em relação a esse processo:
Considerando-se as etapas necessárias para o estabelecimento da especiação a partir de populações originais e a importância desse processo evolutivo na diversidade da vida, é possível afirmar:
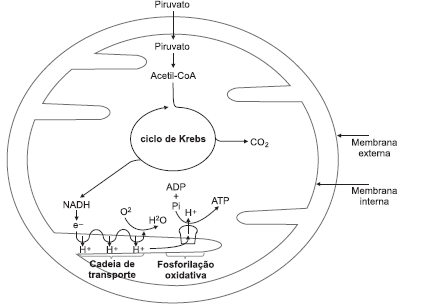
A figura ilustra algumas etapas de determinadas reações oxidativas presentes em células eucarióticas.
Em relação a esse processo e às reações associadas a ele,
é possível afirmar:
O esquema ilustra as etapas da divisão celular por meiose em organismos de padrão eucarionte.
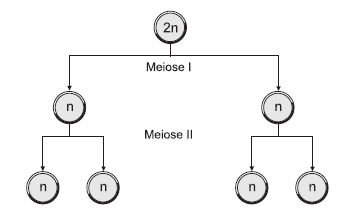
A partir da compreensão dessas etapas e da importância desse mecanismo de divisão para a diversificação da vida, é correto afirmar:
A respeito da importância do estabelecimento de uma sustentabilidade ecológica para a preservação da vida que habita o planeta, é correto afirmar:
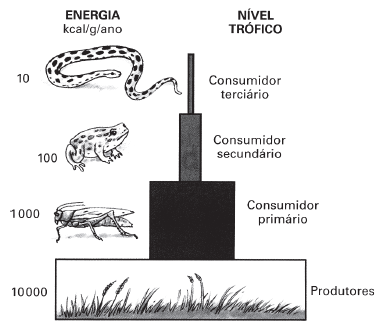
A ilustração representa uma pirâmide de energia de uma determinada cadeia alimentar.
Em relação a essa pirâmide, pode-se afirmar que
O modo como ocorreu a evolução dos processos sexuados e dos ciclos de vida nas plantas foi de fundamental importância para a conquista do ambiente terrestre.
Pode-se considerar como um desses fatores evolutivos na
formação do grupo vegetal
O esquema ilustra experimentos, hoje considerados clássicos, do monge Gregor Mendel, utilizando características herdáveis da ervilha-de-cheiro.
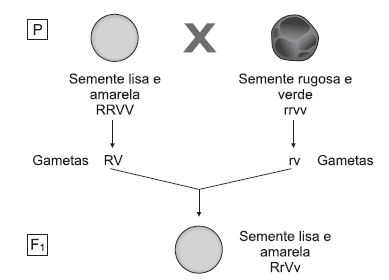
A partir da análise do experimento e do conhecimento a respeito da genética mendeliana, pode-se afirmar:
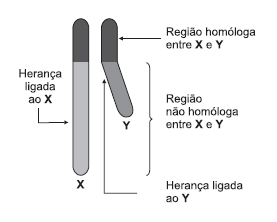
O esquema representa, de forma simbólica, a configuração dos cromossomos sexuais na determinação da herança genética do sexo.
Com base nas informações apresentadas e no conhecimento
atual em relação a esse tipo de herança, pode-se afirmar que a
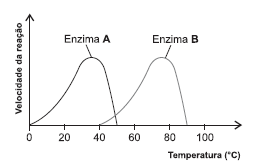
O gráfico representa a variação da velocidade de reação em relação à variação da temperatura do ambiente de duas classes distintas de enzimas.
Considerando-se a análise das informações contidas no
gráfico, pode-se inferir que
A ilustração representa a ação integrada de vários sistemas fisiológicos humanos na manutenção das funções do corpo.
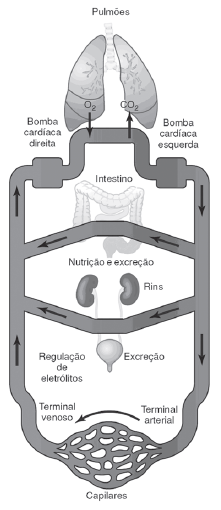
A respeito dessa integração orgânica, é possível afirmar:
O quadro abaixo ilustra a variação da concentração de anticorpos no corpo de um indivíduo em relação ao tempo, como resposta à aplicação em duas doses de uma determinada vacina.
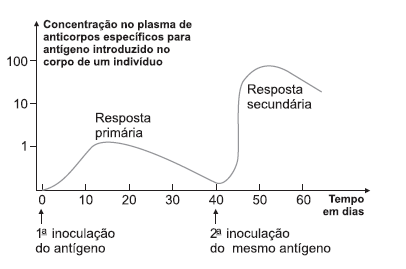
Considerando-se as informações presentes no texto e no gráfico e o conhecimento sobre a importância da vacinação na prevenção de doenças, é possível afirmar:
A partir da análise do texto, do conhecimento sobre o tema e do impacto gerado por esse tipo de experimento na sociedade em geral, pode-se afirmar que