Questões de Vestibular de Química - Eletroquímica: Oxirredução, Potenciais Padrão de Redução, Pilha, Eletrólise e Leis de Faraday.
Foram encontradas 416 questões
Empregado em processos de cromação, o tríóxido de crômio, que é altamente tóxico, corrosivo e carcinogênico, é eventualmente utilizado para a produção de crômio, de acordo com a seguinte reação: 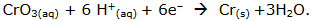
Considerando a reação acima, é correto dizer que a massa, em g, de crômio depositada por 24.125 C é,
aproximadamente
Tendo como referência as informações precedentes, julgue o item que se segue.
Na reação III, há redução do ferro em um processo que
envolve a transferência de dois mols de elétrons por mol
de FeO.
Fonte: https://ucmp.berkeley.edu/glossary/gloss3/pigments.html (acessado em 02/05/2019).
As palavras que completam as lacunas, na ordem em que se encontram no texto, são:
I. No cátodo ocorre a formação de um gás.
II. No ânodo observa-se a liberação de um gás utilizado nas estações de tratamento de água.
III. O pH da solução resultante, após a eletrólise, é menor que 7.
Está/Estão correta(s) apenas a(s) afirmativa(s)