Questões de Vestibular de Química - Cinética Química
Foram encontradas 51 questões
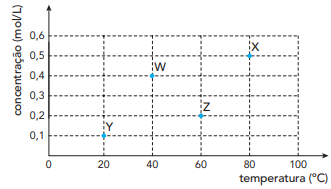
A maior velocidade inicial de formação de gás hidrogênio foi verificada no seguinte experimento:
A reação de decomposição do ozônio é representada pela equação a seguir:
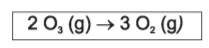
Num dado experimento de decomposição do ozônio, observou-se a variação da concentração molar de O3 em função do tempo, demonstrada no quadro abaixo.

Analisando os dados experimentais, a velocidade
média de produção de gás oxigênio (O2), em
mol/L.minuto, nos 3 minutos iniciais da reação é:
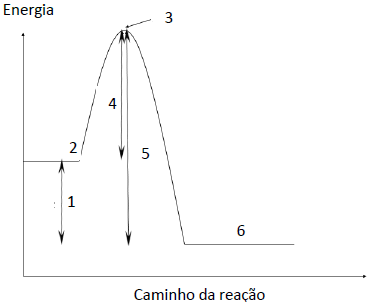
Energia de ativação, variação de entalpia da transformação e complexo ativado podem ser, respectivamente, associados aos números
I. A velocidade de uma reação é uma grandeza que indica como as quantidades de reagentes e produtos dessa reação variam em uma escala temporal. II. A velocidade das reações química depende da concentração dos reagentes. III. Quanto maior for a concentração de reagentes, menor será a velocidade das reações químicas. IV. Em uma reação química, a energia de ativação corresponde ao valor mínimo de energia que as moléculas de reagentes devem possuir para que seja eficaz uma colisão entre elas. V. O valor específico da energia de ativação em uma reação química é uma constante comum a todos os tipos de reações que podem ocorrer. VI. O aumento da temperatura, em uma reação química, contribui para o aumento da velocidade desta reação. VII. Uma substância caracterizada como catalisadora, aumenta a velocidade de uma reação química e, portanto, será, sem exceções, consumida durante a reação. VIII. Um catalisador aumenta a velocidade de uma reação química, pois promove aumento da energia de ativação da mesma. IX. Em uma reação química, a alteração na velocidade devido à ação de um catalisador é denominado catálise.
Na correção dessas afirmações feitas pelo aluno na prova, o professor descontou 2 pontos por cada afirmação incorreta. Sendo assim, pode-se considerar que foi descontado na prova do referido aluno:
Numa determinada condição experimental e com o catalisador adequado, ocorre uma reação, conforme representada no gráfico, que relaciona porcentagem do composto pelo tempo de reação.
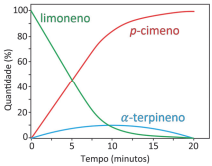
Uma representação adequada para esse processo é: