Questões de Concurso Para engenheiro júnior - processamento
Foram encontradas 135 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2018
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2018 - Transpetro - Engenheiro Júnior - Processamento (Químico) |
Q1090277
Engenharia Química e Química Industrial
O Primeiro Princípio da Termodinâmica, princípio da conservação da energia, relaciona a variação de energia interna de um sistema com o calor e trabalho. Um gás está
contido num cilindro com êmbolo móvel, a uma pressão
de 6,0.104
N/m2. São fornecidos ao sistema 10 kJ de calor
à pressão constante, e o volume do gás sofre uma expansão de 50 L.
O trabalho realizado e a variação de energia interna nessa transformação em Joule, são, respectivamente,
Dado 1 Pa = 1 N m-2
O trabalho realizado e a variação de energia interna nessa transformação em Joule, são, respectivamente,
Dado 1 Pa = 1 N m-2
Ano: 2018
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2018 - Transpetro - Engenheiro Júnior - Processamento (Químico) |
Q1090276
Engenharia Química e Química Industrial
O reator abaixo ilustra um Reator CSTR (Reator Tanque Agitado Contínuo). A reação A → B + C ocorre nesse reator.
A carga inicial é alimentada com uma mistura equimolar de A e inerte à temperatura de 400 K e pressão total de 10 atm.
A vazão de entrada é 8 L/s. Os dados coletados no laboratório e processados foram colocados na Tabela abaixo.
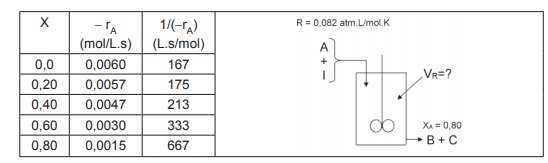
Usando os dados da Tabela e utilizando a Lei dos Gases Ideais, conclui-se que o volume do reator CSTR (em litros) necessário para alcançar uma conversão de 80% é

Usando os dados da Tabela e utilizando a Lei dos Gases Ideais, conclui-se que o volume do reator CSTR (em litros) necessário para alcançar uma conversão de 80% é
Ano: 2018
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2018 - Transpetro - Engenheiro Júnior - Processamento (Químico) |
Q1090275
Engenharia Química e Química Industrial
A Equação de Arrhenius, k = k0
exp(-E/RT), pode ser escrita na forma logarítmica gerando a expressão ln k = ln k0
– E/RT. Os
dados apresentados na Tabela a seguir referem-se à reação 2A → 2B + C.
T (°C) T (K) K (L mol-1 s-1) ln k 161,63 434,78 148,42 5,00 104,20 377,35 1 0 60,18 333,33 0,0067 -5,0
A partir desses dados plotados na Figura abaixo, calcula-se a Energia de Ativação desta reação.
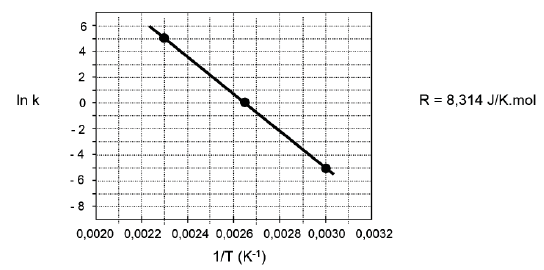
O valor da Energia de Ativação expresso em Joules/mol é
T (°C) T (K) K (L mol-1 s-1) ln k 161,63 434,78 148,42 5,00 104,20 377,35 1 0 60,18 333,33 0,0067 -5,0
A partir desses dados plotados na Figura abaixo, calcula-se a Energia de Ativação desta reação.

O valor da Energia de Ativação expresso em Joules/mol é
Ano: 2018
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2018 - Transpetro - Engenheiro Júnior - Processamento (Químico) |
Q1090274
Engenharia Química e Química Industrial
O tempo espacial expressa o tempo necessário para processar um volume de reator considerando-se a alimentação do fluido nas condições de entrada. Considere um
reator tubular de 200 L que é alimentado com uma vazão
volumétrica de 5 L/s.
O tempo espacial, em minutos, é
O tempo espacial, em minutos, é
Ano: 2018
Banca:
CESGRANRIO
Órgão:
Transpetro
Prova:
CESGRANRIO - 2018 - Transpetro - Engenheiro Júnior - Processamento (Químico) |
Q1090273
Engenharia Química e Química Industrial
Usando os conceitos de Entropia (S) aplicados às reações
químicas, observe a reação química 2A(l) + B(s) → 2C(g).
A Entropia dessa reação química varia do seguinte modo: