Questões de Concurso
Comentadas para uneb
Foram encontradas 129 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Como os micro-organismos estão presentes no ambiente e em qualquer material, é preciso garantir as normas de biossegurança e a preservação da qualidade de vida, com a adoção de medidas de desinfecção e esterilização de materiais.
Considerando-se as características dos processos de desinfecção e esterilização, é correto afirmar:
O pH do solo influencia também na coloração das flores de algumas espécies de plantas, a exemplo das hortênsias, que, em solos ácidos, produzem flores azuis e, em solos alcalinos, flores cor de rosa.
Considerando-se as informações do texto e a relação entre o valor de pH é a concentração de íons H3O+ e OH− , em soluções aquosas, é correto concluir:
Os fertilizantes utilizados no cultivo agrícola são obtidos a partir de substâncias extraídas da natureza ou produzidos em escala industrial, a exemplo do nitrato de amônio, NH4NO3(s), e do diidrogeno-fosfato de cálcio, Ca(H2PO4)2(s).
Com relação às propriedades dos sais inorgânicos utilizados como fertilizantes, é correto afirmar:
Considerando-se esses modelos, é correto afirmar:
Considerando-se as informações do texto, as propriedades dos elementos químicos e suas posições na Tabela Periódica, é correto afirmar:
Os sistemas químicos são porções de matéria separadas para observação e análise, a exemplo dos representados em I, II e III. Esses sistemas podem ser abertos, fechados ou isolados e, assim, trocar ou não matéria e energia com o ambiente.
Considerando-se essas informações e as propriedades dos sistemas apresentados e de seus componentes, é correto afirmar:
Com relação à quebra de seção, é correto afirmar que
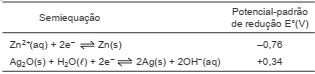
A pilha de zinco e óxido de prata é usada em aparelhos auditivos e relógios de pulso e são menos poluentes do que a de zinco e óxido de mercúrio.
Tendo em vista essas informações e os dados da tabela de
potencial-padrão de redução para as semiequações que
ocorrem nessa pilha, é correto afirmar:
Cr2O2-7 (aq) + Cℓ− (aq) + H+ (aq) → Cr3+(aq) + H2O(ℓ) + Cℓ2(g)
No balanceamento de equações de oxirredução, algumas espécies transferem elétrons para outras, de forma que, no final da reação química, o número de elétrons transferidos é igual ao de elétrons recebidos.
Com base nessas informações e após o balanceamento da equação química com os menores coeficientes estequiométricos inteiros, é correto afirmar:
I. 2H+(aq) + 1/2O2(aq) + 2e- → H2O(ℓ) Eºred = + 1,23v
II. Fe3+(aq) + e- → Fe2+(aq) Eºred = +0,77
As soluções aquosas ácidas de sais de íons Fe2+(aq) são esverdeadas quando recém-preparadas e, quando em contato prolongado com o ar, tornam-se amareladas.
A partir dessas considerações e das semiequações I e II
com os respectivos potenciais-padrão de redução, é correto
afirmar:
O conceito de pH é muito importante para a química, principalmente na análise e correção de solos e na determinação da acidez da água de criatórios de peixes. O sucesso nessas atividades depende da determinação do pH de amostras de soluções preparadas nos laboratórios ou coletadas diretamente no campo. A mistura de 80,0mL de solução, contendo ácido clorídrico 2,50.10−1 molL−1 , com 20,0mL de uma solução de hidróxido de sódio, 5,0.10−1 molL−1 poderá resultar em uma solução final ácida ou básica, a depender das concentrações de uma ou de outra espécie química em solução.
A análise da solução final com base na determinação do pH e de suas propriedades permite corretamente concluir:
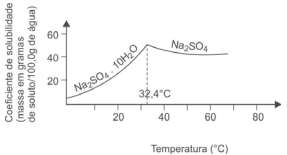
Enquanto algumas substâncias absorvem calor durante a dissolução em água, outras liberam energia ao se dissolverem, como é possível verificar a partir de análise das curvas de solubilidade em função de temperatura. Entretanto existem substâncias que apresentam comportamento semelhante, porém descritos por curvas com “pontos de inflexão”, como a do gráfico de variação do coeficiente de solubilidade, em função da temperatura, do sulfato de sódio decaidratado, Na2SO4.10H2O, em água.
A partir da análise desse gráfico, que representa a
solubilidade em água do sulfato de sódio decaidratado, é
correto afirmar:
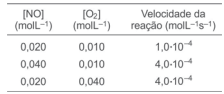
Utilizando-se de experimentos bastante elaborados, os químicos têm investigado o percurso das reações químicas, com o objetivo de determinar a expressão da lei da velocidade e verificar se essas reações são elementares ou não elementares. A tabela apresenta as concentrações colhidas durante três experimentos envolvendo a reação do monóxido de nitrogênio, NO(g), com o oxigênio, O2(g), na obtenção de dióxido de nitrogênio, NO2(g), à determinada temperatura.
A partir da análise dos dados da tabela e das informações
do texto, é correto afirmar que a
Na produção de picles, uma espécie de conserva, legumes, a exemplo de cebola, cenoura e pepino, são colocados durante alguns dias em uma salmoura, NaCl(aq). Após o período, são notadas alterações no sabor e na textura dos alimentos.
Com base nos efeitos dos solutos sobre as propriedades dos líquidos, é correto afirmar:
CH4(g) + 2O2(g) → CO2(g) + 2H2O(g) ΔHo = − 890kJ
A energia elétrica proveniente de biomassa é uma alternativa amplamente utilizada por grandes empresas do agronegócio nas regiões sul e sudoeste. A energia produzida não somente atende às necessidades dos empreendimentos, como também é vendida a concessionárias na região. A fermentação de restos de vegetais e de dejetos de animais coletados nas fazendas de pecuária e de suinocultura é processada em biodigestores e produz biogás, uma mistura gasosa de metano, CH4(g), sulfeto de hidrogênio, H2S(g) e dióxido de carbono, CO2(g), dentre outros gases, e resíduos ricos em bionutrientes usados como fertilizantes na propriedade rural. A combustão do metano, mostrada pela equação química, libera calor utilizado na geração de energia elétrica.
De acordo com essas informações sobre o processo de
geração de energia a partir de biomassa, e
considerando-se o calor específico da água 4,2Jg−1
K−1
, é
correto afirmar:
A água pesada, D2O(ℓ), é um líquido, à temperatura ambiente, utilizado na refrigeração de alguns tipos de reatores nucleares.
Em relação a essa informação, é correto afirmar:
I. 
II. CaNCN(s) + 5H2O(ℓ) → CaCO3(s) + 2NH4OH(aq)
Quando o carbeto de cálcio, CaC2(s), é aquecido em forno elétrico na presença de nitrogênio, forma-se cianamida de cálcio, CaNCN, de acordo com a equação química I. Esse composto é largamente empregado como fertilizante nitrogenado de ação lenta porque se hidrolisa em alguns meses, quando comparado ao nitrato de amônio, NH4NO3, e ureia, H2NCONH2, que são arrastados facilmente pelas chuvas.
A compreensão dessas informações com base nos conhecimentos de Química permite corretamente afirmar:
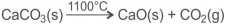
O calcário é um minério que contém carbonato de cálcio, CaCO3. É utilizado na agricultura para corrigir o pH do solo e na produção de cal, CaO, destinada à indústria siderúrgica, de cimento, de vidro e de alvejantes.
Uma amostra de 30,0g de calcário foi calcinada a 1100ºC e liberou 6,0L de dióxido de carbono, CO2(g), medidos a 30ºC e 1,0atm.
A partir dessas informações sobre a calcinação da amostra de calcário, é correto afirmar:
Durante o aquecimento de um tubo teste contendo uma mistura de solução de nitrato de amônio, NH4NO3(aq) e de hidróxido de sódio NaOH(aq) recém-preparadas, há desprendimento de um gás irritante de odor característico.
Levando-se em consideração os resultados dessa experiência e com base nas propriedades dessa substância química, é correto afirmar que esse gás