Questões de Concurso
Foram encontradas 2.448 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Q2388271
Química
Niels Bohr realizou cálculos de energias associadas às
órbitas permitidas para o elétron no átomo de hidrogênio
isolado. As energias calculadas ajustam-se à fórmula
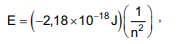
onde E é a energia da órbita permitida para um elétron no átomo de hidrogênio, em Joule, e n representa o número quântico principal que assume valores inteiros de 1, 2, 3, ... ∞ .
Dessa forma, com base nesse modelo atômico, para Bohr a(o)
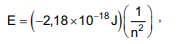
onde E é a energia da órbita permitida para um elétron no átomo de hidrogênio, em Joule, e n representa o número quântico principal que assume valores inteiros de 1, 2, 3, ... ∞ .
Dessa forma, com base nesse modelo atômico, para Bohr a(o)
Q2388264
Química
Na soldagem por aluminotermia, representada na reação
a seguir, a reação do alumínio com um óxido metálico produz óxido de alumínio, com liberação de calor e deposição de Fe.
8Al (s) + 3Fe3 O4(s) = 9Fe(s) + 4Al 2 O3(s) + CALOR
Considere 100,0 g de alumínio de soldagem com pureza de 81% e que a reação tem 75% de rendimento, por causa da troca de calor com o ambiente.
A quantidade de ferro, em gramas, formada nesse processo é, aproximadamente, de
8Al (s) + 3Fe3 O4(s) = 9Fe(s) + 4Al 2 O3(s) + CALOR
Considere 100,0 g de alumínio de soldagem com pureza de 81% e que a reação tem 75% de rendimento, por causa da troca de calor com o ambiente.
A quantidade de ferro, em gramas, formada nesse processo é, aproximadamente, de
Q2388263
Química
O reagente de Pierce é usado na determinação de enxofre e sulfeto de carbono em óleo. A preparação envolve a
dissolução de 1,00 g de sulfato de cobre(II) pentahidratado em 15 mL de água, adicionando-se, em seguida,
4 mL de solução de hidróxido de amônio e 3 g de cloridrato de hidroxilamina. Essa mistura foi diluída com água,
ajustando o volume final para 50,00 mL. Dessa solução,
uma alíquota de 10,00 mL foi coletada.
A quantidade mais próxima, em milimol, de cobre nessa alíquota de solução é igual a
A quantidade mais próxima, em milimol, de cobre nessa alíquota de solução é igual a
Q2388261
Química
Uma solução foi formada a partir da mistura das seguintes
soluções aquosas:
• 500 mL de solução de fluoreto de magnésio com concentração 0,020 mol L-1
• 200 mL de solução de fluoreto de alumínio com concentração 3,36 g L-1
• 300 mL de solução de fluoreto de sódio com concentração 0,060 mol L-1
Admitindo-se que os solutos estão completamente dissociados, a concentração de íons fluoreto, em mol L-1 , na solução resultante da mistura é igual a
Dado
Al = 27 g mol-1 F = 19 g mol-1
• 500 mL de solução de fluoreto de magnésio com concentração 0,020 mol L-1
• 200 mL de solução de fluoreto de alumínio com concentração 3,36 g L-1
• 300 mL de solução de fluoreto de sódio com concentração 0,060 mol L-1
Admitindo-se que os solutos estão completamente dissociados, a concentração de íons fluoreto, em mol L-1 , na solução resultante da mistura é igual a
Dado
Al = 27 g mol-1 F = 19 g mol-1
Q2388259
Química
Um procedimento foi desenvolvido para a determinação
de íons cálcio em uma solução aquosa. A uma alíquota
de 200 mL dessa solução foi adicionado excesso de ácido
oxálico (H2
C2
O4
). Em seguida, adicionou-se amônia, de
modo a precipitar todo o cálcio presente na amostra na
forma de oxalato de cálcio. O precipitado foi filtrado, seco
e calcinado, de acordo com a seguinte reação:
CaC2 O4 (s) → CaO (s) + CO (g) + CO2 (g)
Após o resfriamento, a massa de óxido de cálcio na amostra foi de 112 mg.
A concentração de íons cálcio, em g L-1 , na solução aquosa é
Dado Ca = 40 g mol-1 , C = 12 g mol-1 , O = 16 g mol-1
CaC2 O4 (s) → CaO (s) + CO (g) + CO2 (g)
Após o resfriamento, a massa de óxido de cálcio na amostra foi de 112 mg.
A concentração de íons cálcio, em g L-1 , na solução aquosa é
Dado Ca = 40 g mol-1 , C = 12 g mol-1 , O = 16 g mol-1