Questões de Concurso
Foram encontradas 836 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210804
Química
A autoionização da água é um processo muito importante, pois dependendo da sua posição de equilíbrio
químico, define-se a acidez (ou alcalinidade) das soluções aquosas. Através de experimentos de condutividade
elétrica da água pura e da sua condutância específica, é possível determinar o grau de ionização da água e,
posteriormente, a constante de equilíbrio, Kw, da reação de autoionização. A 25 °C, o valor de Kw é 1,00 x 10-14
.
Por outro lado, para a água pura, a 37 °C, o grau de ionização é 73% maior, tendo em vista que a autoionização
da água é endotérmica. Vale ressaltar que nesta variação de temperatura a concentração molar da água é
praticamente invariável.
Diante das informações e a partir dos seus conhecimentos, assinale a opção que mostra aproximadamente O VALOR DO pOH de uma solução de pH 8,50, a 37 °C:
Dados: densidade da água = 1000 g/L; massa molar da água = 18 g/mol; log(1,73) = 0,24; log(3) = 0,48.
Diante das informações e a partir dos seus conhecimentos, assinale a opção que mostra aproximadamente O VALOR DO pOH de uma solução de pH 8,50, a 37 °C:
Dados: densidade da água = 1000 g/L; massa molar da água = 18 g/mol; log(1,73) = 0,24; log(3) = 0,48.
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210797
Química
O ácido hialurônico (AH) é uma macromolécula de origem natural, presente em diversos tecidos do corpo
humano, principalmente na pele, cartilagens, líquido sinovial e humor vítreo do olho. É um glicosaminoglicano
composto por unidades repetidas do dissacarídeo formado pela N-acetilglicosamina e o ácido D-glicurônico
(Figura abaixo).
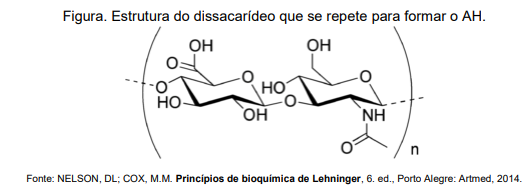
O AH é altamente hidrofílico e capaz de reter grandes quantidades de água, o que lhe confere propriedades viscoelásticas e lubrificantes. Na pele, por exemplo, ele é responsável por manter a hidratação e elasticidade, além de ajudar a preencher o meio extracelular, o que contribui para a uniformidade da superfície cutânea.
Sobre a química do AH e a partir dos seus conhecimentos, assinale a opção CORRETA:

O AH é altamente hidrofílico e capaz de reter grandes quantidades de água, o que lhe confere propriedades viscoelásticas e lubrificantes. Na pele, por exemplo, ele é responsável por manter a hidratação e elasticidade, além de ajudar a preencher o meio extracelular, o que contribui para a uniformidade da superfície cutânea.
Sobre a química do AH e a partir dos seus conhecimentos, assinale a opção CORRETA:
Ano: 2023
Banca:
COPESE - UFPI
Órgão:
UFPI
Prova:
COPESE - UFPI - 2023 - UFPI - Técnico de Laboratório - Química |
Q2210795
Química
O termo “superácido” é usado para descrever os ácidos mais fortes do que o ácido sulfúrico, um dos ácidos
comuns mais fortes. George Andrew Olah (1927 - 2017), um químico húngaro-estadunidense, ganhou o Prêmio
Nobel de Química em 1994, com a aplicação de superácidos ao estudo de carbocátions. A água é um solvente
incapaz de distinguir os superácidos do ácido sulfúrico, uma vez que ela apresenta o chamado “efeito nivelador”.
Portanto, na quantificação da acidez dos superácidos é comum o uso da função de acidez de Hammett, H0, que
é definida matematicamente como:
H0 = pKa(BH+) - log [BH+] / [B]
onde B é um indicador básico, BH+ é o ácido conjugado desse indicador e pKa(BH+) é a constante de acidez deste último. Quando o indicador é nitroanilina (C6H6N2O2), experimentos realizados para ácidos puros nas mesmas condições, permitem construir a tabela abaixo:
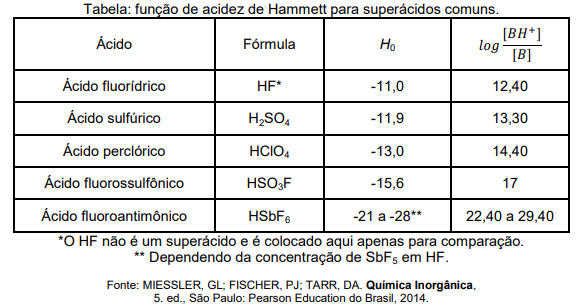
Diante dessas informações, assinale a opção que mostra a ÚNICA reação termodinamicamente espontânea entre pares das substâncias citadas acima:
H0 = pKa(BH+) - log [BH+] / [B]
onde B é um indicador básico, BH+ é o ácido conjugado desse indicador e pKa(BH+) é a constante de acidez deste último. Quando o indicador é nitroanilina (C6H6N2O2), experimentos realizados para ácidos puros nas mesmas condições, permitem construir a tabela abaixo:

Diante dessas informações, assinale a opção que mostra a ÚNICA reação termodinamicamente espontânea entre pares das substâncias citadas acima:
Ano: 2023
Banca:
FGV
Órgão:
SEDUC-TO
Prova:
FGV - 2023 - SEDUC-TO - Professor da Educação Básica - Professor Regente - Química |
Q2206539
Química
Em um recipiente fechado à determinada temperatura, o equilíbrio 2SO3(g) ⇆ 2SO2(g) + O2(g) é estabelecido com as pressões parciais de SO2 (g) e O2 (g) iguais, respectivamente a 0,8 atm e a 0,4 atm. A pressão total do sistema é de 1,4 atm.
Assinale a opção que indica o valor da constante de equilíbrio em função das pressões.
Assinale a opção que indica o valor da constante de equilíbrio em função das pressões.
Ano: 2023
Banca:
SELECON
Órgão:
IF-RJ
Prova:
SELECON - 2023 - IF-RJ - Técnico de Laboratório/Química |
Q2175677
Química
A solubilidade de uma determinada dibase foi determinada
por um técnico de laboratório, após introduzi-la em uma solução de pH 12. Sabe-se que o Kps, da base em questão, vale 32.10-12 a 25º C. Assim, o valor da solubilidade encontrada, em mol/L, após
os cálculos foi de: