Questões de Concurso
Foram encontradas 836 questões
Resolva questões gratuitamente!
Junte-se a mais de 4 milhões de concurseiros!
( ) A análise gravimétrica é um método analítico em que são utilizadas somente medições de massa e informações sobre estequiometria de reação para determinar a quantidade de um analito em uma amostra.
( ) Um precipitado deve apresentar as seguintes características no produto final: ter composição conhecida e constante, não ser higroscópico, ser formado de partículas pequenas, ser muito puro e pouco solúvel.
( ) Precipitados são formados por dois processos: por nucleação e por crescimento de partículas.
( ) A filtração é a separação da fase sólida contendo o precipitado desejado da solução-mãe utilizando papel de filtro combinado com funil de vidro, ou, mais comumente, cadinhos filtrantes de vidro sinterizado.
( ) A peptização é um processo no qual os compostos normalmente solúveis são removidos da solução por um precipitado.
A ordem correta de preenchimento dos parênteses, de cima para baixo, é:
Um frasco contém uma mistura em equilíbrio de X2(g) e X atômico, segundo a reação:
X2(g) ⇌ 2 X(g)
A pressão de equilíbrio encontrada foi de 2,4 atm em certa condição de temperatura e volume. Se X2 gasoso a
uma pressão parcial de 3 atm for adicionado à mistura em equilíbrio acima, a volume e temperatura constantes,
a nova pressão de equilíbrio será de 5,66 atm, sendo que, no processo, a pressão do X (g) atômico aumenta
65% em relação ao valor da condição inicial. Nestas condições, assinale a opção que mostra O VALOR MAIS
PRÓXIMO DE Kp para a decomposição de X2(g), na mesma temperatura:
Figura: Curvas dos valores de frações em mol para: ácido carbônico - linha pontilhada; bicarbonato - linha tracejada; carbonato - linha sólida.
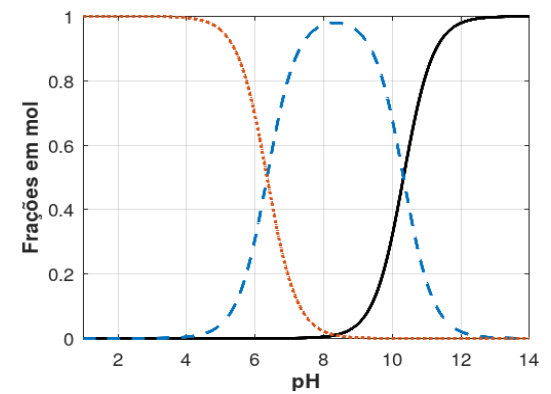
A partir das informações acima e sabendo que o Kps (constante produto de solubilidade) do CaCO3(s) (Calcita) é 4,5 x 10-9 , a 25°C , assinale a opção que mostra o valor aproximado da SOLUBILIDADE MOLAR deste carbonato, em pH 10: Dados eventualmente necessários:√4,5 = 2,12; √6,25 = 2,5; √3 = 1,73; √5 = 2,24; √10 = 3,16; √20 = 4,47.