Questões de Concurso Público IF-PR 2023 para Técnico de Laboratório - Química
Foram encontradas 10 questões
Q2186951
Química
Diversos óleos essenciais, utilizados como flavorizantes naturais, possuem componentes que são opticamente ativos.
Esses pares de isômeros apresentam odores e sabores diferentes que variam com o poder de desviar o plano da luz
polarizada para a esquerda (isômero levógiro) ou para a direita (isômero dextrógiro). Em alguns casos, a medição
experimental do ângulo do desvio permite identificar a fonte natural do flavorizante. O equipamento necessário para
fazer essa determinação é o:
Q2186952
Química
A quantificação de persulfato de potássio no produto comercial denominado “pó descolorante” pode ser feita por
iodometria, segundo a seguinte equação:
S2O8 –2 + 3 I– → 2 SO4 –2 + I3 –
A velocidade dessa reação, determinada experimentalmente, é expressa por:
v = k.[S2O8 –2].[I–]
Em relação ao exposto, assinale a alternativa que apresenta corretamente a ordem global da reação direta.
S2O8 –2 + 3 I– → 2 SO4 –2 + I3 –
A velocidade dessa reação, determinada experimentalmente, é expressa por:
v = k.[S2O8 –2].[I–]
Em relação ao exposto, assinale a alternativa que apresenta corretamente a ordem global da reação direta.
Q2186953
Química
A dependência da constante de equilíbrio de uma reação com a temperatura pode ser exemplificada pelo aumento da
constante do produto de ionização da água (Kw) com a temperatura, como indicado no quadro a seguir:
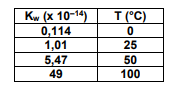
Considerando os dados apresentados, assinale a alternativa que contém a afirmativa correta.

Considerando os dados apresentados, assinale a alternativa que contém a afirmativa correta.
Q2186954
Química
Na análise espectrofotométrica de Fe+3, contido em ácido clorídrico concentrado, esse íon é extraído com éter etílico
[(C2H5)2O], e o cloreto férrico (FeCl3) é recuperado pela evaporação do solvente. A interação dos íons metálicos com o
éter pode ser explicada pela equação a seguir:
Dados: d(HCl 37%) = 1,19 g/mL; d(éter etílico) = 0,713 g/mL
Fe+3 + (C2H5)2O + HCl → (C2H5)2OH+. FeCl4[(C2H5)2O]2 –
Considerando a técnica descrita, o equipamento correto para realizar a extração é o:
Dados: d(HCl 37%) = 1,19 g/mL; d(éter etílico) = 0,713 g/mL
Fe+3 + (C2H5)2O + HCl → (C2H5)2OH+. FeCl4[(C2H5)2O]2 –
Considerando a técnica descrita, o equipamento correto para realizar a extração é o:
Q2186955
Química
As celas galvânicas com celas separadas podem ser representadas graficamente da seguinte maneira:
A0│A+n ║ B+n│B0
em que A0 e B0 são as espécies A e B reduzidas, A+n e B+n são as espécies A e B oxidadas, o símbolo │ corresponde à interface metal/solução, e a representação ║ é a ponte salina.
Considerando que pilhas com celas separadas necessitam de uma ponte salina para funcionar, a função dessa ponte salina no conjunto é de:
A0│A+n ║ B+n│B0
em que A0 e B0 são as espécies A e B reduzidas, A+n e B+n são as espécies A e B oxidadas, o símbolo │ corresponde à interface metal/solução, e a representação ║ é a ponte salina.
Considerando que pilhas com celas separadas necessitam de uma ponte salina para funcionar, a função dessa ponte salina no conjunto é de: