Questões de Concurso Público UFPR 2018 para Químico
Foram encontradas 40 questões
Q925953
Química
A fórmula química de um composto representa sua composição em termos de símbolos químicos dos elementos que
compõem uma determinada substância. A xantofila, uma substância encontrada em penas de aves e em flores, contém
átomos de carbono, hidrogênio e oxigênio na razão 20:28:1. Sabendo que uma molécula desse composto tem seis átomos
de oxigênio, qual é a fórmula química da xantofila?
Q925954
Química
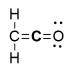
A molécula orgânica ceteno (C2H2O) tem a seguinte estrutura de Lewis:
Q925955
Química
O avanço nas técnicas de análises de espécies químicas diversas permite o descobrimento de fenômenos importantes,
como o ocorrido com a espectrometria de massas, técnica que permitiu identificar que átomos de um mesmo elemento
podem apresentar massas diferentes. Essa observação foi definitiva para o refinamento do modelo nuclear, com a
descoberta de uma nova partícula subatômica – o nêutron – e a identificação de isótopos. Considere a seguinte tabela:
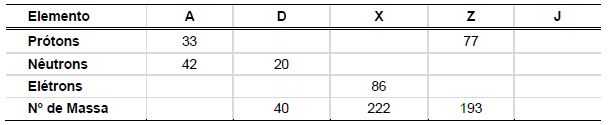
Supondo que os elementos A, D, X, Z e J possam ocorrer na forma de isótopos, e com base nas informações contidas na tabela, é correto afirmar que:

Supondo que os elementos A, D, X, Z e J possam ocorrer na forma de isótopos, e com base nas informações contidas na tabela, é correto afirmar que:
Q925956
Química
Alguns núcleos são instáveis e tendem a sofrer
decaimento até que um núcleo mais estável seja
formado. Esses núcleos decaem uma série de
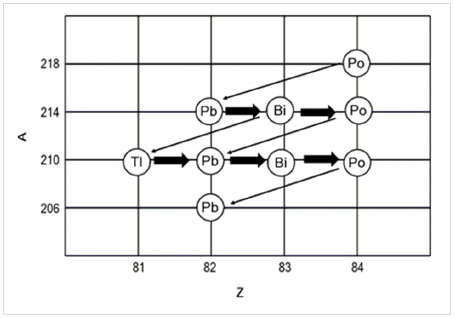
etapas e dão origem a uma série radioativa. Na
figura a seguir, está mostrado o decaimento do 218Po até 206Pb.
Com relação a decaimento, considere as seguintes equações:
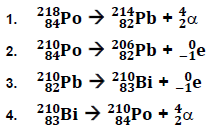
São equações de decaimento:
Com relação a decaimento, considere as seguintes equações:
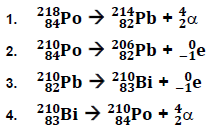

São equações de decaimento:
Q925957
Química
Uma solução foi preparada pela dissolução de 500 mg de cloreto de potássio, 500 mg de sulfeto de potássio e 500 mg de
fosfato de potássio em 500 mL de água. Qual é a concentração final, em mol L-1
, de íons potássio em solução? (Massas
molares (g mol-1
): O = 16; P = 31; S = 32; Cl = 35,5; K = 39,1)