Questões de Concurso Público UFRJ 2014 para Técnico em Química
Foram encontradas 12 questões

Levando em consideração os algarismos significativos, o volume correto lido da proveta é:
(1) 40 mL de uma solução de NaOH foi totalmente neutralizada com 16 mL de uma solução de HCl.
(2) Depois, 55 mL de NaOH foram adicionados a uma quantidade de matéria de 0,046 mols de ácido acético.
(3) O excesso de NaOH da etapa 2 foi titulada com uma solução de HCl e foram gastos 8,25 mL do ácido até o ponto de equivalência.
Com base nessas anotações, o volume de NaOH necessário para neutralizar 0,046 mols de CH3COOH é de:
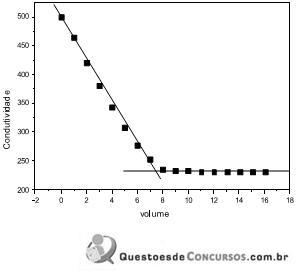
Atente-se que para a primeira reta, a equação obtida foi: y = -23,291 x + 456,64 e para a segunda reta, a equação obtida foi: 231,8.
Baseado nessas informações, é correto afirmar que o volume do ácido necessário para alcançar o ponto de equivalência e a concentração do ácido é respectivamente: