Questões de Concurso Público INT 2024 para Tecnologista Pleno - Biocatálise
Foram encontradas 4 questões
Ano: 2024
Banca:
Instituto Access
Órgão:
INT
Prova:
Instituto Access - 2024 - INT - Tecnologista Pleno - Biocatálise |
Q2470916
Química
Sabe-se que a reação de oxidação da glicose pela glicose oxidase
segue uma cinética michaeliana e que os valores da constante de
afinidade e da velocidade de reação para um sistema com
concentração de substrato igual a 0,5 mmolL-1 são 2mmolL-1 e 50
mmolL-1min-1, respectivamente. Pergunta-se: qual é o valor da
velocidade máxima de formação dos produtos?
Ano: 2024
Banca:
Instituto Access
Órgão:
INT
Prova:
Instituto Access - 2024 - INT - Tecnologista Pleno - Biocatálise |
Q2470917
Química
O modelo cinético de Michaelis e Menten é válido se as
determinações forem feitas em condições iniciais. Isso porque
I. há excesso de substrato em relação à concentração de enzima;
II. a concentração do complexo enzima-substrato produzido é imediatamente consumido;
III. as concentrações de enzima e substrato se modificam consideravelmente.
Analise os itens acima e assinale
I. há excesso de substrato em relação à concentração de enzima;
II. a concentração do complexo enzima-substrato produzido é imediatamente consumido;
III. as concentrações de enzima e substrato se modificam consideravelmente.
Analise os itens acima e assinale
Ano: 2024
Banca:
Instituto Access
Órgão:
INT
Prova:
Instituto Access - 2024 - INT - Tecnologista Pleno - Biocatálise |
Q2470926
Química
As enzimas são moléculas de proteínas com grande massa molar.
Essas moléculas, entretanto, atuam de maneira altamente específica
e agem como catalisadoras biológicas de apenas uma única reação.
Reações de cinética enzimática são comumente representadas por
gráficos que apresentam informações importantes, como a
velocidade da reação, o aumento da concentração do produto na
reação e a taxa de saturação da enzima, entre outras. O uso de
gráficos também nos permite avaliar o aumento e a diminuição da
atividade enzimática por moléculas ativadoras e inibidoras que se
ligam especificamente às enzimas. Assim, o gráfico abaixo mostra a
cinética enzimática na presença de dois agentes inibidores (X, Y).
Com relação a esse gráfico, avalie as afirmativas a seguir.
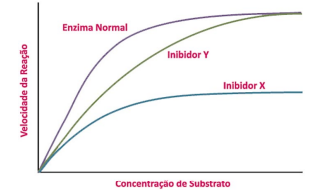
I. Na curva da reação cinética da enzima normal, os valores de V0 aumentam rapidamente com baixas concentrações de substrato e passam a se nivelar em um platô com altas concentrações desse mesmo substrato. Esse platô ocorre porque todas as moléculas da enzima disponíveis se encontram ligadas ao substrato e quaisquer moléculas adicionais do substrato terão que aguardar ser processadas até que outra molécula dessa enzima se torne disponível. Por isso, a velocidade da reação é limitada pela concentração da enzima e o seu valor máximo, ou Vmax, é o valor da velocidade inicial de reação no qual a enzima normal atinge o platô.
II. O inibidor X é um inibidor competitivo porque retarda o progresso da reação ao se ligar à enzima, que ocorre geralmente no sítio ativo, impedindo que o verdadeiro substrato se ligue. Portanto, o inibidor e o substrato competem pela enzima. A inibição competitiva age diminuindo o número de moléculas enzimáticas disponíveis para se ligar ao substrato.
III. O inibidor Y é um inibidor não competitivo, porque não impede que o substrato se ligue à enzima. O inibidor e o substrato não interferem na capacidade um do outro de se ligar à enzima. Contudo, quando o inibidor está ligado, a enzima não é capaz de catalisar a reação para gerar um produto. Portanto, a inibição não competitiva age reduzindo o número de moléculas funcionais da enzima que pode realizar a reação.
Assinale

I. Na curva da reação cinética da enzima normal, os valores de V0 aumentam rapidamente com baixas concentrações de substrato e passam a se nivelar em um platô com altas concentrações desse mesmo substrato. Esse platô ocorre porque todas as moléculas da enzima disponíveis se encontram ligadas ao substrato e quaisquer moléculas adicionais do substrato terão que aguardar ser processadas até que outra molécula dessa enzima se torne disponível. Por isso, a velocidade da reação é limitada pela concentração da enzima e o seu valor máximo, ou Vmax, é o valor da velocidade inicial de reação no qual a enzima normal atinge o platô.
II. O inibidor X é um inibidor competitivo porque retarda o progresso da reação ao se ligar à enzima, que ocorre geralmente no sítio ativo, impedindo que o verdadeiro substrato se ligue. Portanto, o inibidor e o substrato competem pela enzima. A inibição competitiva age diminuindo o número de moléculas enzimáticas disponíveis para se ligar ao substrato.
III. O inibidor Y é um inibidor não competitivo, porque não impede que o substrato se ligue à enzima. O inibidor e o substrato não interferem na capacidade um do outro de se ligar à enzima. Contudo, quando o inibidor está ligado, a enzima não é capaz de catalisar a reação para gerar um produto. Portanto, a inibição não competitiva age reduzindo o número de moléculas funcionais da enzima que pode realizar a reação.
Assinale
Ano: 2024
Banca:
Instituto Access
Órgão:
INT
Prova:
Instituto Access - 2024 - INT - Tecnologista Pleno - Biocatálise |
Q2470927
Química
Os ensaios de atividade enzimática são, na sua maioria, realizados
para identificar a presença ou a quantidade de uma enzima
específica em um organismo, tecido ou qualquer outra amostra
biológica. Por isso, vários reagentes e variadas metodologias estão
amplamente disponíveis e permitem a investigação de interações
específicas entre enzima e substrato. A atividade enzimática pode
ser avaliada por vários métodos, como PCR convencional, análise do
perfil eletroforético das amostras em gel de agarose, ensaios
enzimáticos com sondas fluorogênicas e também a zimografia.
A zimografia, no entanto, é um método versátil e amplamente utilizado para avaliar o perfil de proteínas de um substrato. Com isso, a zimografia pode ser adaptada para investigar diferentes enzimas, substratos e sistemas biológicos, contribuindo para a compreensão de processos metabólicos, regulação enzimática e diagnóstico de doenças. Considerando os princípios, tipos, usos e aplicações da técnica de zimografia, assina a afirmativa incorreta.
A zimografia, no entanto, é um método versátil e amplamente utilizado para avaliar o perfil de proteínas de um substrato. Com isso, a zimografia pode ser adaptada para investigar diferentes enzimas, substratos e sistemas biológicos, contribuindo para a compreensão de processos metabólicos, regulação enzimática e diagnóstico de doenças. Considerando os princípios, tipos, usos e aplicações da técnica de zimografia, assina a afirmativa incorreta.