Questões de Concurso Público IF-MS 2019 para Química
Foram encontradas 20 questões
(COSTA, T.S. et al. Confirmando a esterificação de Fischer por meio dos aromas. Química Nova na Escola, n. 19, p. 36-38, Maio de 2004).
Na esterificação de 1 mol de ácido acético com 1 mol de álcool etílico num recipiente de 1 litro, a 25 °C, o equilíbrio é atingido com constante de equilíbrio igual a 4. Dessa forma, qual a quantidade em mols do éster presente no equilíbrio?
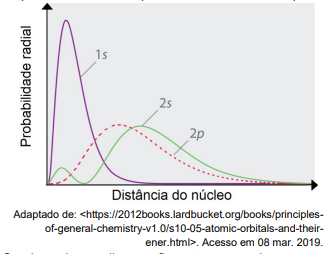
Sendo assim, analise as afirmações a seguir e assinale a alternativa correta:
I. Os orbitais 2s e 2p são degenerados. II. Os orbitais 2s têm uma maior capacidade de penetração do que os orbitais 2p. III. Os orbitais 2p são menos blindados pelos elétrons dos orbitais 1s, quando comparados aos orbitais 2s. IV. Um átomo com configuração eletrônica terminada em ns1 tem menor energia de ionização quando comparado a um outro átomo com configuração eletrônica terminada em ns2np1.
Dados das massas molares em g.mol-1 : C = 12 e O = 16.
Dados: R = 8,31 J.K-1 .mol-1 ; ln 2 = 0,7
SnS + HCℓ + HNO3 → SnCℓ4 + S + NO + H2O
Após o balanceamento da equação, a soma total dos coeficientes mínimos e inteiros das espécies envolvidas na reação é
Para que um átomo de tório com número de massa igual a 228 se desintegre espontaneamente para formar um átomo, do mesmo elemento químico com número de massa igual a 220, os números de partículas alfa e beta que deverão ser emitidas, respectivamente, são:
Reação 1: ΔH1 = +15,3 kJ/mol e ΔS1 =+30 J/K.mol Reação 2: ΔH2 = +1,8 kJ/mol e ΔS2 =-159 J/K.mol.
Escolha a alternativa que representa os valores de ΔG1 e ΔG2 em kJ/mol, respectivamente, e as previsões corretas de espontaneidade ou não espontaneidade da reação nessa temperatura:
(Santos, W.; Mol, G. S. Química cidadã, vol. 1, 2ª ed., São Paulo: Editora AJS, 2013.)
Assinale a alternativa que apresenta, respectivamente, um óxido: básico, ácido, neutro e anfótero:
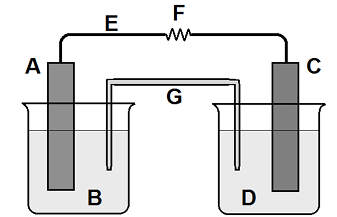
Legenda da figura: (A) placa de estanho, (B) solução aquosa contendo íons Sn2+, (C) placa de alumínio, (D) solução aquosa contendo íons Aℓ3+, (E) fio metálico, (F) resistência elétrica e (G) ponte salina.
Considerando os seguintes dados:
E°(Sn2+/Sn) = -0,14 V E°(Aℓ3+/Aℓ) = -1,68 V
Durante o funcionamento da pilha, o estudante fez algumas afirmações:
I. A concentração de íons alumínio aumenta na solução da direita (D). II. Na placa de alumínio ocorre a corrosão. III. O fluxo de elétrons ocorre pelo fio metálico a partir da placa de estanho em direção à placa de alumínio. IV. Na placa de estanho ocorre a redução. V. A placa de estanho é o polo negativo da cela galvânica.
Dessas afirmações,
Considerando que uma amostra de 2,0 kg, contendo 80% de óxido de cobre II, foi utilizada para reagir com o ácido citado no livro de Stephen King. Admitindo que os outros compostos da amostra não reagem com o ácido, determine a massa aproximada de ácido necessária para que todo o cobre da amostra sofra reação química.
Considere as seguintes massas molares em g.mol-1 : Cu = 63,5; O = 16; H = 1 e S = 32.
Dados: log 2 = 0,30 e log 3 = 0,48
(Atkins, P.W.; Jones, L. Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente. Ed 5, Bookman, 2011.)
Sobre titulação, assinale a alternativa correta:
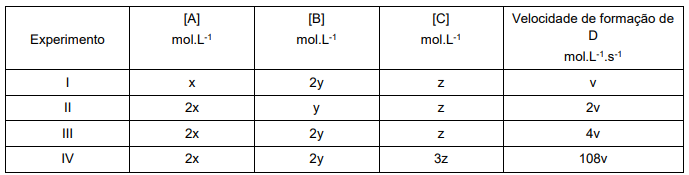
Determine a velocidade da reação em função de v se as concentrações de A, B e C, forem, respectivamente, igual a: 3x, 5y e 2z.
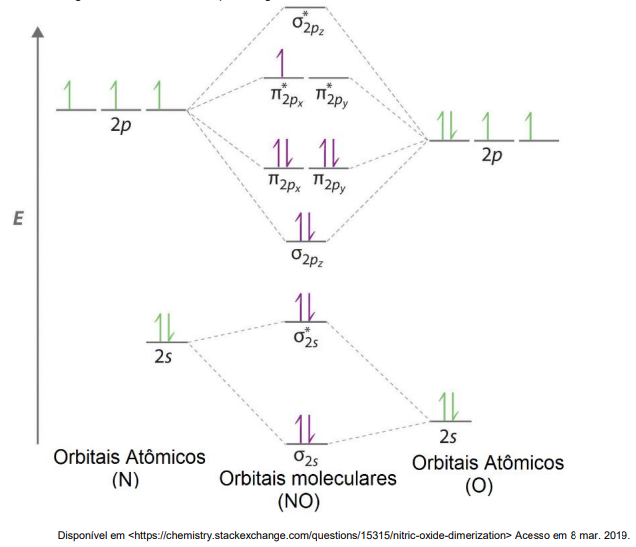
Sendo assim, escolha a alternativa que representa quais características serão apresentadas no íon NO+ .
Programa espacial da NASA busca vida alienígena no 2º maior satélite do Sistema Solar (25/02/2019). Disponível em Acesso em 8 mar. 2019
Sobre as propriedades físico-químicas dos compostos orgânicos, assinale a afirmativa correta:
(Atkins, P.W.; Jones, L. Princípios de Química: Questionando a Vida Moderna e o Meio Ambiente. Ed. 5, Bookman, 2011.)
Dessa forma, assinale a alternativa correta: