Questões de Concurso Público IF-BA 2014 para Técnico de Laboratório - Química
Foram encontradas 47 questões
Ano: 2014
Banca:
FUNRIO
Órgão:
IF-BA
Prova:
FUNRIO - 2014 - IF-BA - Técnico de Laboratório - Química |
Q586168
Química
Texto associado
Em meados do século XVIII, começaram os estudos sistemáticos de identificação de compostos pelo uso de chamas. A
origem das cores geradas pela presença de metais nas chamas está na estrutura eletrônica dos átomos. As chamas podem ser
usadas para a identificação qualitativa de cátions, ilustrando o uso dos testes de chama. A tabela abaixo reúne uma coloração
típica de chamas, devido à presença de alguns cátions em estado excitado.
Coloração típica de chamas devido à presença de alguns cátions em estado excitado
Elemento Cor da chama Elemento Cor da chama
Antimônio Azul-esverdeada Cobre Verde
Arsênio Azul Estrôncio Vermelho-tijolo
Bário Verde-amarelada Lítio Carmin
Cálcio Alaranjada Potássio Violeta
Chumbo Azul Sódio Amarela
Coloração típica de chamas devido à presença de alguns cátions em estado excitado
Elemento Cor da chama Elemento Cor da chama
Antimônio Azul-esverdeada Cobre Verde
Arsênio Azul Estrôncio Vermelho-tijolo
Bário Verde-amarelada Lítio Carmin
Cálcio Alaranjada Potássio Violeta
Chumbo Azul Sódio Amarela
(Revista Química Nova na Escola, N23, maio, 2006.)
Dessa forma, a coloração típica de chamas pode ser explicada pelo:
Ano: 2014
Banca:
FUNRIO
Órgão:
IF-BA
Prova:
FUNRIO - 2014 - IF-BA - Técnico de Laboratório - Química |
Q586169
Química
Texto associado
Alguns dizem que o hidrogênio é o combustível do futuro. Além do alto poder calorífico, o produto da combustão é água,
não poluente portanto. Os métodos mais comuns de preparação do hidrogênio em laboratório são a reação de ácidos diluídos
com metais ou a de um álcali com alumínio, tendo como exemplos, respectivamente:
Zn + H
2SO4 → ZnSO4 + H2
2Al + 2 NaOH + 6 H2O → 2 Na[Al(OH)4] + 3H2
Considerando a produção de hidrogênio em um laboratório via reação de ácidos diluídos com metais, os nomes do ácido e do
sal do exemplo acima são, respectivamente:
Ano: 2014
Banca:
FUNRIO
Órgão:
IF-BA
Prova:
FUNRIO - 2014 - IF-BA - Técnico de Laboratório - Química |
Q586170
Química
A qualidade dos combustíveis é verificada por meio de testes específicos que revelam se os produtos estão de acordo com as
especificações estabelecidas pela Agência Nacional do Petróleo -ANP e, também se houve adição ilegal de solventes. O teste
de teor de álcool presente na gasolina, conforme disposto na Resolução ANP nº 9, de 7 de março de 2007 é feito com solução
aquosa de cloreto de sódio ( NaCl) na concentração de 10% p/v. O cálculo do teor de álcool é determinado pela expressão:
T= (A X 2) +1, Onde: T = Teor de álcool na gasolina e A = aumento em volume da fase aquosa. Considerando um teor
permitido de álcool na gasolina de 25%, pode-se dizer que uma amostra analisada pelo Teste da Proveta ao obter um
aumento em volume de 30 mL da fase aquosa:
Ano: 2014
Banca:
FUNRIO
Órgão:
IF-BA
Prova:
FUNRIO - 2014 - IF-BA - Técnico de Laboratório - Química |
Q586171
Química
As formulações de detergentes mais atuais substituíram os catalisadores usuais por enzimas, catalisadores biológicos, pois a
maioria dos usuais agredia o meio ambiente, sendo tóxicos e provocavam o desgaste de materiais e de instrumentos. Estas
enzimas têm a grande vantagem de serem 100% biodegradáveis. Dessa forma, uma nova geração de detergentes sem fosfato
e sem cloro alvejante, contendo apenas enzimas, com formulação mais segura e menos cáustica, tem sido utilizada, mas com
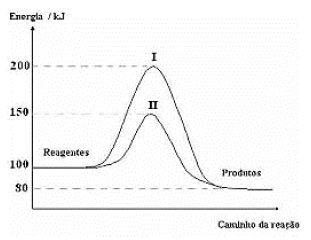
o mesmo desempenho. O gráfico abaixo exemplifica o efeito de um catalisador sobre a rapidez de uma mesma reação
química. Após a análise do gráfico pode-se afirmar que:

Ano: 2014
Banca:
FUNRIO
Órgão:
IF-BA
Prova:
FUNRIO - 2014 - IF-BA - Técnico de Laboratório - Química |
Q586172
Química
Uma solução tampão de qualquer pH desejado pode ser preparada pela combinação de quantidades calculadas de um par
ácido-base conjugado adequado. Na prática, porém, os valores de pH de tampões preparados em laboratório utilizando
quantidades teóricas diferem dos valores previstos, por conta de incertezas nos valores numéricos de muitas constantes de
dissociação e das simplificações utilizadas nos cálculos. Em virtude disso, é comum se prepararam tampões gerando uma
solução cujo pH seja aproximadamente aquele desejado, e então o ajustam pela adição de um ácido forte ou base forte até
que o pH requerido seja indicado por um pH-metro. Assim, para preparar 500 mL de uma solução tampão com pH= 5,00 a
partir do ácido acético (HOAc) e acetato de sódio (NaOAc) 1,00 mol/L, a concentração e a massa de acetato de sódio
respectivamente devem ser aproximadamente iguais a: (Dados: ka = 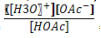 = 1,75 x 10-5 e Massa molar de
NaOAc = 82,034 g )
= 1,75 x 10-5 e Massa molar de
NaOAc = 82,034 g )
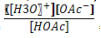 = 1,75 x 10-5 e Massa molar de
NaOAc = 82,034 g )
= 1,75 x 10-5 e Massa molar de
NaOAc = 82,034 g )