Questões de Concurso Público SEDUC-PE 2016 para Professor de Química
Foram encontradas 50 questões
Q701278
Química
O ácido benzoico foi descoberto no século XVI e recebeu esse
nome por ter sido extraído do benjoeiro.
Em 1875, Salkowski verificou que esse ácido atua como fungicida
e, desde então, o ácido benzoico vem sendo usado como
germicida na preservação de alimentos e como adjuvante
farmacológico anti-fúngico, normalmente em concentrações que
variam entre 0,05 a 0,15%. Trata-se de um composto de fórmula
molecular C7H6O2
(massa molar = 122 g.mol -1
) pouco solúvel em
água.
Em uma solução aquosa, comporta-se como um ácido fraco, com
pKa = 4.
Uma solução aquosa de ácido benzoico em concentração 0,12%
(m/v) apresenta pH aproximadamente igual a
Q701279
Química
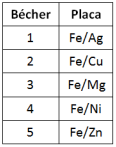
Em um ensaio de corrosão, placas bimetálicas (Fe/Ag, Fe/Cu,
Fe/Mg, Fe/Ni e Fe/Zn) foram dispostas em diferentes bécheres
contendo água do mar, conforme o esquema a seguir:
Considere a tabela a seguir.
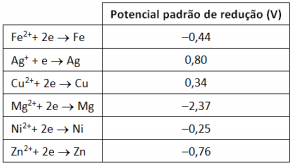
Após o mesmo tempo de observação, o bécher em que se verifica a menor taxa de corrosão da placa de ferro é o

Considere a tabela a seguir.

Após o mesmo tempo de observação, o bécher em que se verifica a menor taxa de corrosão da placa de ferro é o
Q701280
Química
Em um laboratório foi montada uma aparelhagem para
recolhimento do gás oxigênio produzido na reação de
decomposição do clorato de potássio, como ilustra a figura a
seguir.
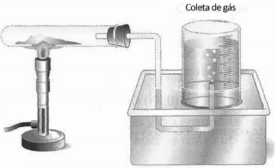
A reação observada pode ser representada pela equação: 2 KClO3 → 2 KCl + 3 O2 Uma amostra de clorato de potássio foi parcialmente decomposta sendo a pressão do gás recolhido de 0,8 atm e seu volume de 180 mL na temperatura de 27ºC. Considerando o comportamento ideal do gás, a massa de clorato de potássio que sofreu decomposição foi de, aproximadamente, Dados: Massa Molar: KClO3 = 122,5 g.mol-1 Constante real dos gases R= 0,082atm.L.mol-1 .K-1

A reação observada pode ser representada pela equação: 2 KClO3 → 2 KCl + 3 O2 Uma amostra de clorato de potássio foi parcialmente decomposta sendo a pressão do gás recolhido de 0,8 atm e seu volume de 180 mL na temperatura de 27ºC. Considerando o comportamento ideal do gás, a massa de clorato de potássio que sofreu decomposição foi de, aproximadamente, Dados: Massa Molar: KClO3 = 122,5 g.mol-1 Constante real dos gases R= 0,082atm.L.mol-1 .K-1
Q701281
Química
O tecnécio é um dos elementos mais utilizados em medicina
nuclear e seu isótopo 99mTc, um gama emissor, é utilizado em
exames de imagens. Uma solução contendo 99mTc é ingerida ou
injetada no paciente e através da radiação gama emitida, os
médicos podem obter imagens de órgãos como coração, fígado e
pulmões.
Doze horas após a aplicação da solução de 99mTc, foi detectado
em um paciente 1/4 da atividade inicial desse isótopo. Após
24horas de aplicação, a porcentagem que restará no paciente
será de
Q701282
Química
É mais fácil para um nêutron se aproximar de um núcleo alvo do que um próton. Como o nêutron não tem carga, ele não é repelido pela carga do núcleo e não é necessário acelerá-lo a velocidades muito altas. Um exemplo de transmutação induzida por nêutron é a formação do cobalto-60, que é utilizado no tratamento do câncer, a partir do isótopo de ferro-58. Na primeira etapa ocorre a produção do ferro-59. Na segunda etapa ocorre o decaimento beta(ß) do ferro-59. Na terceira e última etapa ocorre a produção do cobalto-60. (Atkins, P.; Jones, L. Princípio da Química, 3ª Ed. Porto Alegre: Bookman. 2006) A reação total que representa o processo descrito no texto é