Questões de Concurso Público FIOCRUZ 2010 para Tecnologista em Saúde - Flexografia
Foram encontradas 17 questões
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568618
Farmácia
A Resolução - RDC N° 17, de 16 de abril de 2010 “Dispõe
sobre as Boas Práticas de Fabricação de Medicamentos",
preceitua que
“dependendo da função e operação do equipamento, utilidade ou sistema, em determinadas situações, somente se fazem necessárias a __________ e a __________, assim como a operação correta do equipamento, utilidades ou sistemas pode ser considerada um indicador suficiente de seu __________."
De acordo com a legislação em referência, assinale a alternativa que melhor preenche os espaços da sentença.
“dependendo da função e operação do equipamento, utilidade ou sistema, em determinadas situações, somente se fazem necessárias a __________ e a __________, assim como a operação correta do equipamento, utilidades ou sistemas pode ser considerada um indicador suficiente de seu __________."
De acordo com a legislação em referência, assinale a alternativa que melhor preenche os espaços da sentença.
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568620
Farmácia
A Resolução - RDC N° 17, de 16 de abril de 2010 “Dispõe
sobre as Boas Práticas de Fabricação de Medicamentos"
preconiza que a requalificação deve ser realizada de acordo
com um cronograma definido. A freqüência de requalificação
pode ser determinada com base nos seguintes fatores:
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568621
Farmácia
Um aspecto essencial na validação de limpeza é determinar
quanto de limpeza é suficiente. Apesar de oficialmente não
endossar critérios adotados por indústrias farmacêuticas, o
FDA (Food Drug Administration) dos Estados Unidos da
América faz referência a critérios adotados pela empresa Eli
Lilly, que estabelece os seguintes critérios (LeBlanc, 1999):
I. O equipamento deve estar visualmente limpo.
II. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 10 ppm ou 10 mg/g do produto após a limpeza em relação ao produto subseqüente.
III. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 1/100 da dose mínima diária da substância ativa em relação à dose máxima diária do produto subseqüente, calculado de acordo com a equação seguinte (LeBlanc, 1999):
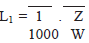
Onde:
L1 = Limite no produto subseqüente em mg/g
Z = Dose mínima diária do produto a ser limpo
Assinale:
I. O equipamento deve estar visualmente limpo.
II. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 10 ppm ou 10 mg/g do produto após a limpeza em relação ao produto subseqüente.
III. Qualquer agente ativo do produto após a limpeza deve estar presente em níveis máximos de 1/100 da dose mínima diária da substância ativa em relação à dose máxima diária do produto subseqüente, calculado de acordo com a equação seguinte (LeBlanc, 1999):
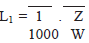
Onde:
L1 = Limite no produto subseqüente em mg/g
Z = Dose mínima diária do produto a ser limpo
Assinale:
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568624
Farmácia
De acordo com a RDC N°17, de 16 de abril de 2010, são
exemplos de itens que devem ser verificados por ocasião da
aplicação do protocolo de Qualificação de Instalação (QI):
Ano: 2010
Banca:
FGV
Órgão:
FIOCRUZ
Prova:
FGV - 2010 - FIOCRUZ - Tecnologista em Saúde - Flexografia |
Q568625
Farmácia
De acordo com o que estabelece a RDC N°17, de 16 de abril
de 2010, o fabricante é responsável pela qualidade dos
medicamentos por ele fabricados, assegurando que sejam
adequados aos fins a que se destinam, cumpram com os
requisitos estabelecidos em seu registro e não coloquem os
pacientes em risco por apresentarem segurança, qualidade
ou eficácia inadequada. O cumprimento deste objetivo é
responsabilidade: