Questões de Química - Transformações Químicas para Concurso
Foram encontradas 457 questões
Ano: 2024
Banca:
CESPE / CEBRASPE
Órgão:
Prefeitura de Joinville - SC
Prova:
CESPE / CEBRASPE - 2024 - Prefeitura de Joinville - SC - Professor de Ciências |
Q2366401
Química
De acordo com suas propriedades físicas e químicas, os
elementos da tabela periódica podem ser classificados em dois
grandes grupos: metais e ametais. Os metais são, geralmente,
brilhantes, são sólidos condutores de eletricidade e são utilizados
em ligas metálicas. Os ametais combinam-se entre si e também
com os metais.
À luz das informações apresentadas, assinale a opção correta.
À luz das informações apresentadas, assinale a opção correta.
Ano: 2024
Banca:
CESPE / CEBRASPE
Órgão:
Prefeitura de Joinville - SC
Prova:
CESPE / CEBRASPE - 2024 - Prefeitura de Joinville - SC - Professor de Ciências |
Q2366400
Química
O químico inglês John Dalton interpretou as leis ponderais das
combinações químicas com base no conceito de átomo, que
significa, em grego, “não divisível”. Dalton fez muitas medidas
das razões das massas dos elementos que se combinavam para
formar compostos e formulou os seus postulados, segundo os
quais
Q2358152
Química
A capsaicina, princípio picante do fruto de várias espécies de pimenta (Capsicum e
Solanaceae), foi isolada em 1876, e sua estrutura foi determinada em 1919. A capsaicina tem
atividade anti-inflamatória e analgésica, por isso, pode ser utilizada para o tratamento de dores
causadas por doenças reumáticas. Em relação à molécula de capsaicina, analise as assertivas a seguir:
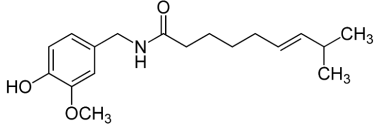
I. Apresenta as funções cetona e amina em sua estrutura.
II. Possui oito átomos de carbono com hibridização sp2 .
III. Apresenta dois carbonos terciários, oito carbonos secundários e dois carbonos primários.
IV. Possui três átomos de carbono com hibridização sp.
V. Apresenta fórmula molecular C18H27NO3.
Quais estão corretas?

I. Apresenta as funções cetona e amina em sua estrutura.
II. Possui oito átomos de carbono com hibridização sp2 .
III. Apresenta dois carbonos terciários, oito carbonos secundários e dois carbonos primários.
IV. Possui três átomos de carbono com hibridização sp.
V. Apresenta fórmula molecular C18H27NO3.
Quais estão corretas?
Ano: 2024
Banca:
FUNCERN
Órgão:
IF-RN
Prova:
FUNCERN - 2024 - IF-RN - Técnico de Laboratório - Área Química |
Q2355888
Química
Texto associado
Uma das funções do Ministério da Agricultura, Pecuária e Abastecimento (MAPA) é a
padronização da qualidade dos alimentos que chegam até a população brasileira por meio de Instruções
Normativas que aprovam regulamentos técnicos que fixam a identidade e as características de qualidade de
um produto. Entre esses produtos estão o leite cru refrigerado, o leite pasteurizado e o leite pasteurizado
tipo A. Esses produtos são regulamentados pela Instrução Normativa MAPA Nº 76, de 26 de novembro de
2018, que, no Art. 5°, define que, entre os parâmetros físico-químicos listados, o leite cru refrigerado deve
apresentar teor mínimo de sólidos totais de 11,4g/100g (11 inteiros e 4 décimos de gramas por 100 gramas)
e acidez titulável entre 0,14 (14 centésimos) e 0,18 (18 centésimos) expressa, em gramas, de ácido
lático/100g.
Segundo o trecho, o teor de acidez titulável em leite deve estar entre 0,14 e 0,18 gramas de ácido láctico/
100g de leite. O técnico do laboratório de química realizou análise de acidez titulável no leite de acordo
com a equação química abaixo e verificou que, em uma amostra de 10mL do leite, gastou 2mL de NaOH
0,1mol/L. Considerando que apenas o ácido láctico esteja presente no leite, então o teor de acidez titulável
em g/100g é (Considere a densidade do leite de 1g/cm3
):
C3H6O3 + NaOH → Na(C3H5O3) + H2O
C3H6O3 + NaOH → Na(C3H5O3) + H2O
Ano: 2023
Banca:
SELECON
Órgão:
SEDUC-MT
Prova:
SELECON - 2023 - SEDUC-MT - Professor de Educação Básica - Química |
Q2336568
Química
A reação química entre sulfato ferroso e permanganato de
potássio em meio ácido é representada pela seguinte reação
química:
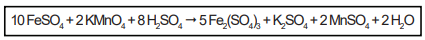
Nessa reação, o elemento químico que sofre oxidação tem como símbolo:
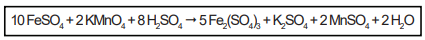
Nessa reação, o elemento químico que sofre oxidação tem como símbolo: